A transposição dos grandes vasos (TGV) é uma cardiopatia congénita cianótica caracterizada pela comutação das grandes artérias. Há 2 apresentações: as formas dextro (D)- e levo (L)-. A forma L-TGV é rara e corrigida no período congénito, porque os ventrículos também estão trocados. A forma D-TGV representa 3% de todos os casos de cardiopatia congénita. A malformação ocorre na fase neonatal da vida com cianose que não responde à oxigenoterapia. O diagnóstico é confirmado com ecocardiograma e um raio-X de tórax que mostra o clássico padrão "ovo preso por um fio". O tratamento é principalmente cirúrgico, e o prognóstico para os casos corrigidos cirurgicamente é bom.
Última atualização: Jan 30, 2025
A transposição dos grandes vasos (TGV) é a comutação das origens dos grandes vasos, em que a aorta surge do ventrículo direito e a artéria pulmonar surge do ventrículo esquerdo.
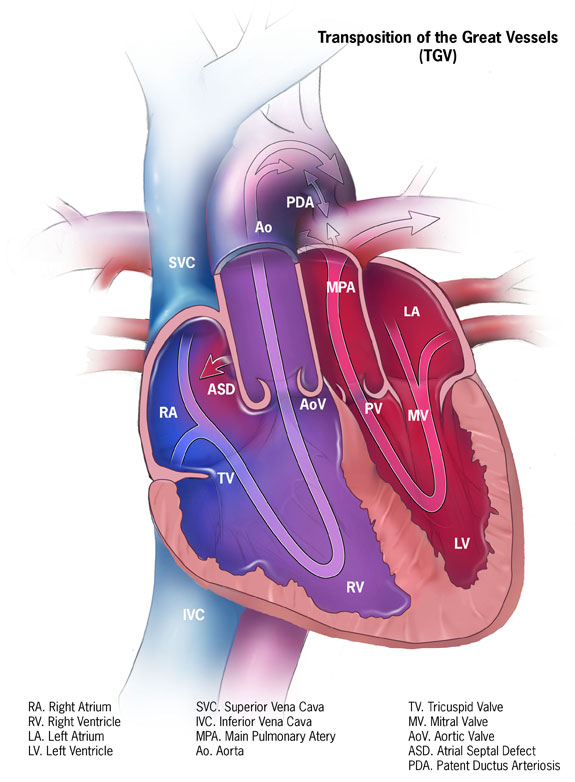
Transposição das grandes vasos
Imagem: “Transposition of the great vessels” por Centers for Disease Control and Prevention. Licença: CC0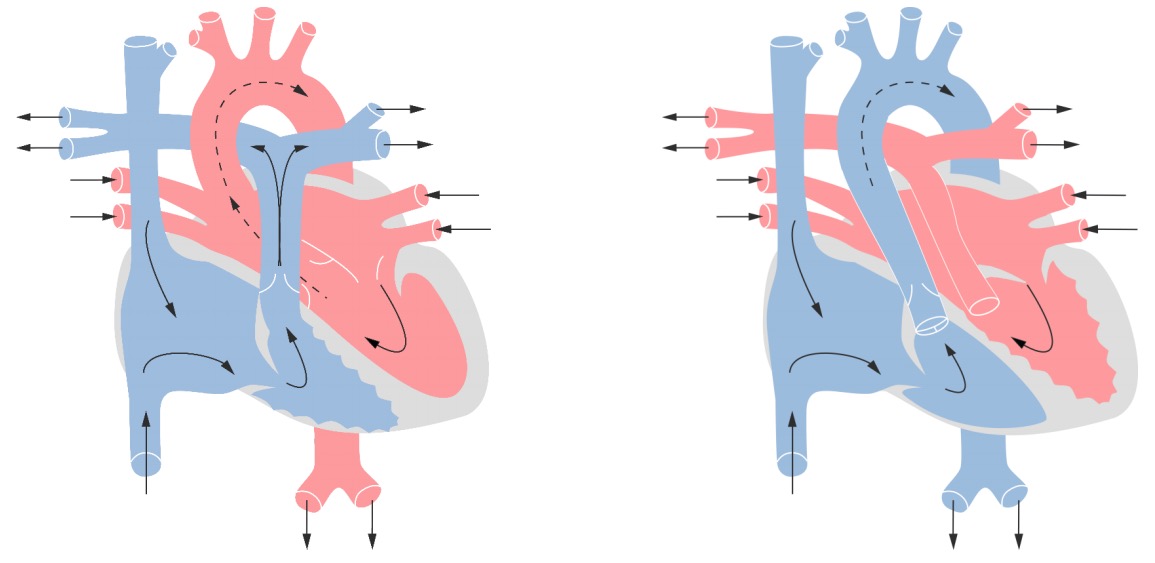
Um coração normal versus o coração de um paciente com TGV
A origem da aorta é no ventrículo direito, que transporta sangue desoxigenado, enquanto a artéria pulmonar tem origem no ventrículo esquerdo.
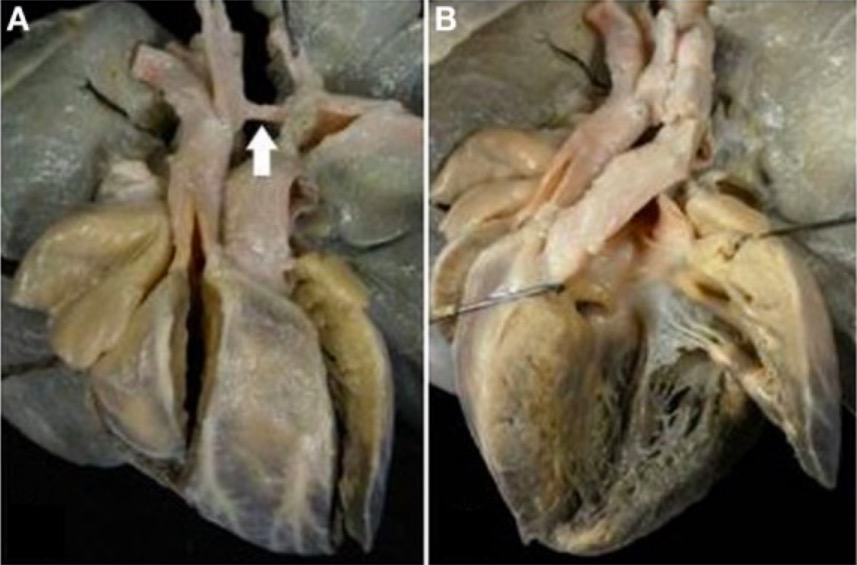
TGV completo com CIV e obstrução do arco aórtico
A: Visão externa do coração mostrando o posicionamento anterior direito da aorta e a hipoplasia grave do arco aórtico entre as artérias carótida e subclávia (seta)
B: A artéria pulmonar tem origem no ventrículo esquerdo. Observe o desalinhamento da CIV com o septo infundibular desviado para a direita.
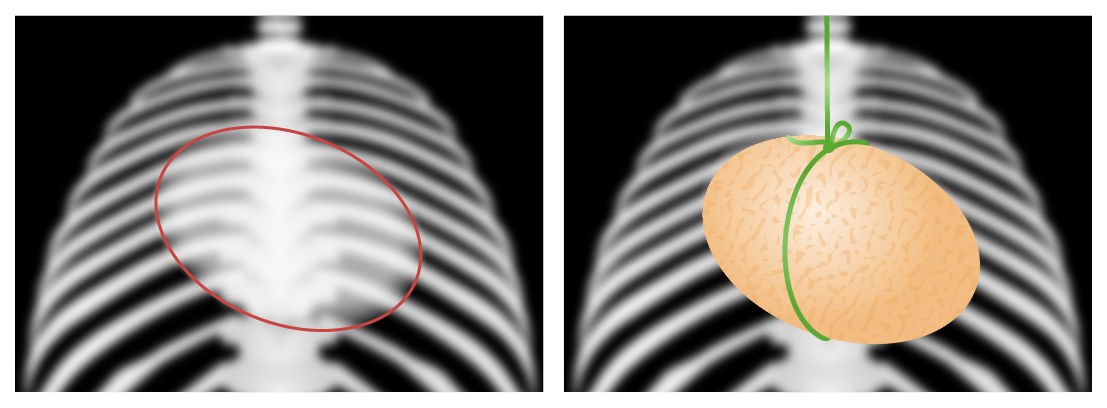
Sinal de ovo preso por um fio
Estas figuras gráficas recriam as imagens radiográficas do tórax de uma criança com transposição dos grandes vasos, conhecido como o “sinal de ovo preso por um fio”. O ovo representa um coração globular cuja aparência se deve à convexidade proeminente do bordo da aurícula direita e à ampliação da aurícula esquerda. O fio representa um exagero da atenuação do mediastino superior que é estreitado devido à atrofia tímica induzida pelo stress (e consequente perda da sombra tímica normalmente proeminente).
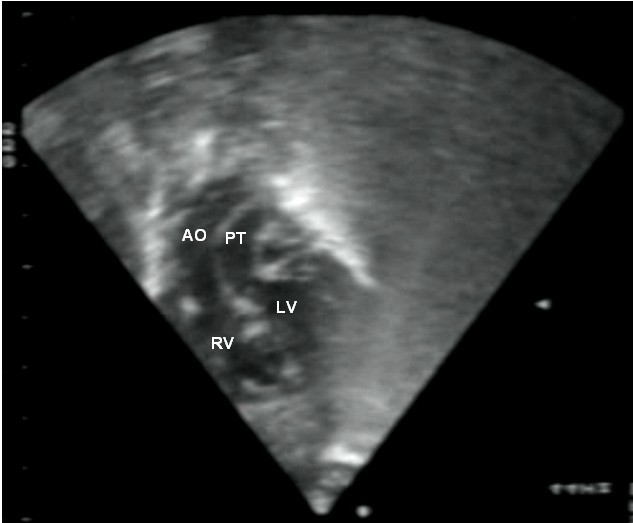
Ecocardiograma mostrando a transposição dos grandes vasos.
Esta visão subcostal mostra conexões arteriais ventriculares discordantes juntamente com a presença de grandes artérias paralelas, ao invés de se cruzarem, que emergem dos ventrículos.
LV: ventrículo esquerdo
RV: ventrículo direito
PT: tronco pulmonar
AO: aorta
Médico:
Cirurgia: