A hipersensibilidade tipo II, também conhecida como hipersensibilidade citotóxica mediada por anticorpos, é causada por anticorpos imunoglobulina G (IgG) e IgM dirigidos contra antigénios nas células ou em materiais extracelulares. Esta reação leva a processos citotóxicos envolvendo anticorpos e o sistema do complemento. Outro mecanismo que ocorre é a interferência na função celular normal, resultando numa disfunção estimulatória ou inibitória. O antigénio desencadeante pode ser intrínseco ou parte da célula hospedeira. Os antigénios extrínsecos como os hemoderivados ou determinados fármacos, podem provocar uma reação semelhante. Para o diagnóstico, são utilizadas análises laboratoriais e procedimentos invasivos, consoante o sistema afetado. O tratamento da doença resultante varia desde cuidados de suporte a antibioterapia, fármacos imunossupressores e cirurgia.
Última atualização: Dec 20, 2024
A ligação dos complexos Ac-antigénio desencadeia os seguintes mecanismos:
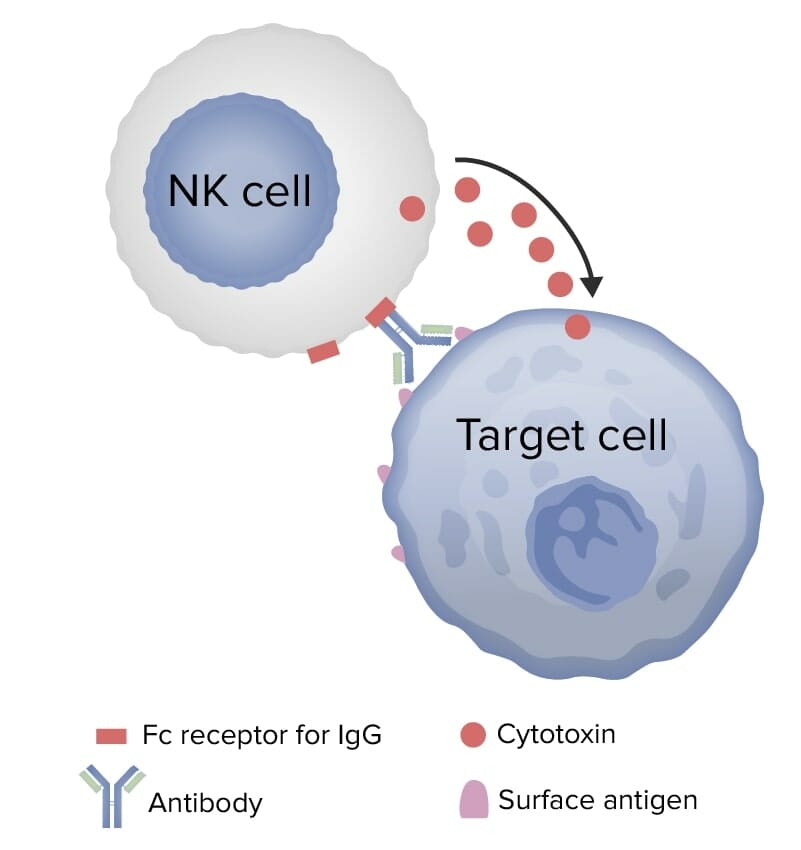
Citotoxicidade celular ou mediada por células dependente de anticorpos:
O anticorpo liga-se aos antigénios de superfície da célula alvo. A célula efetora portadora de Fc (natural killer ou célula NK) liga-se à região Fc do anticorpo e liberta grânulos citotóxicos levando à lise da célula alvo.
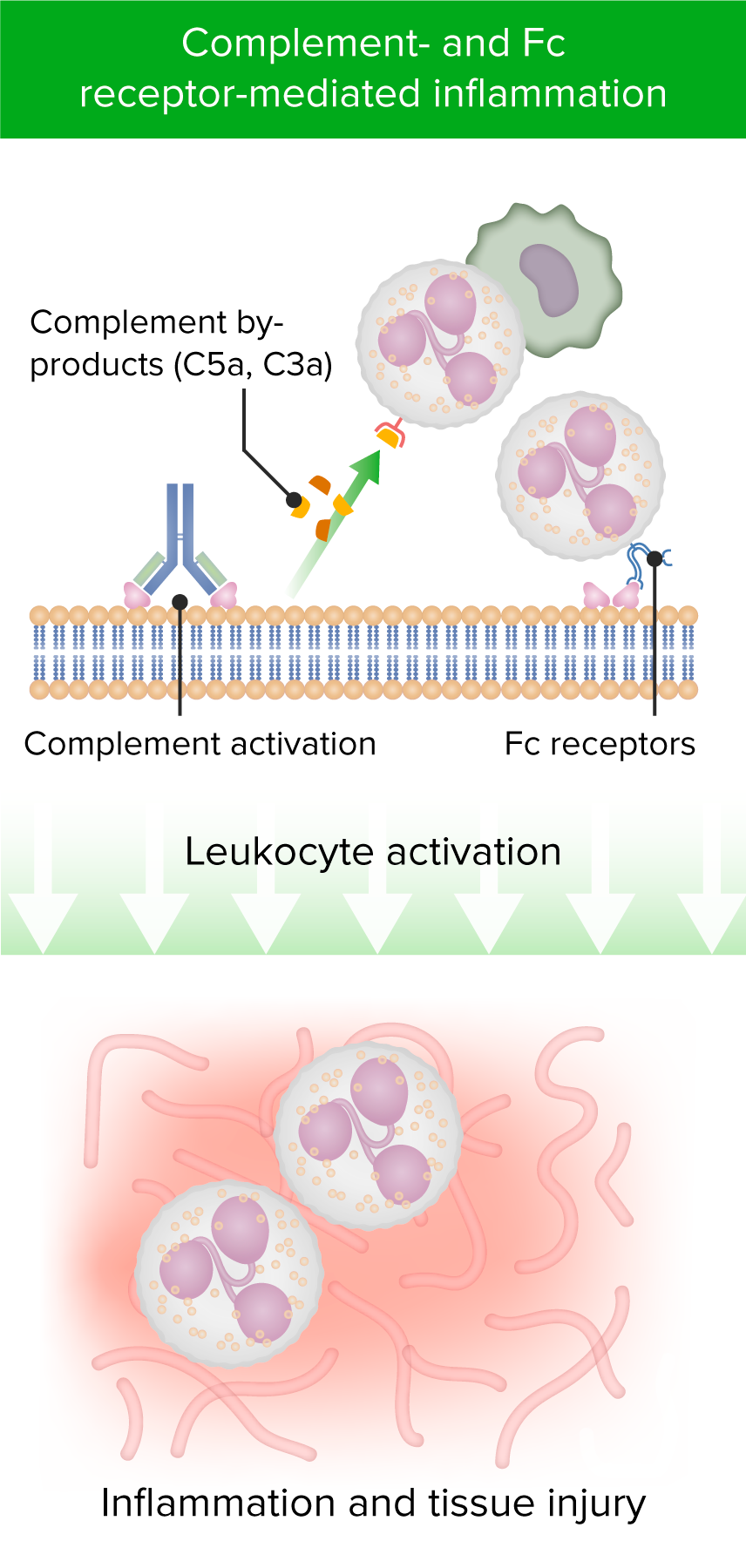
Efeitos mediados por anticorpos (quando um anticorpo se liga à superfície celular):
Ativação do sistema de complemento, de leucócitos e de células efetoras portadoras do recetor Fc, sobretudo as células NK, levando a inflamação e a lesão celular.
A hipersensibilidade tipo II pode resultar das seguintes condições:
Reações transfusionais (incompatibilidade ABO ou de grupo sanguíneo)
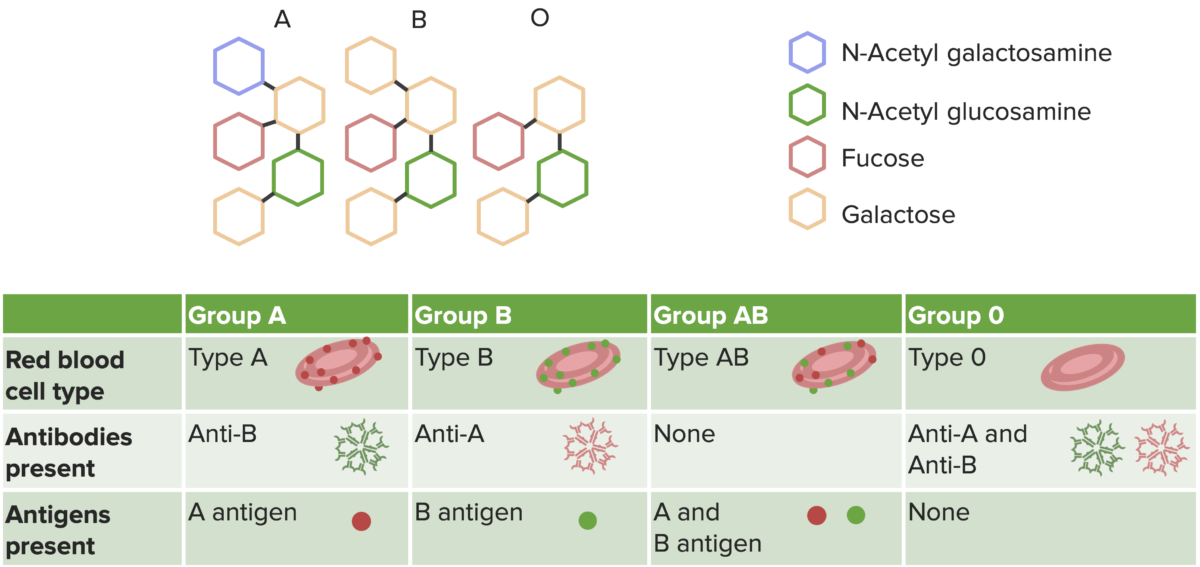
Reações transfusionais induzidas por reações de hipersensibilidade tipo II. Este diagrama mostra os grupos sanguíneos e os seus anticorpos e antigénios correspondentes.
Imagem de Lecturio.Anemia hemolítica autoimune (contra os eritrócitos)
Anemia perniciosa (contra o fator intrínseco)
Doença hemolítica do feto e do recém-nascido (contra eritrócitos; incompatibilidade RhD)
Púrpura trombocitopénica autoimune
Febre reumática aguda
Síndrome de Goodpasture
Doença de Graves
Miastenia gravis
O diagnóstico e o tratamento variam consoante as manifestações clínicas, o sistema orgânico envolvido e a gravidade do comprometimento causada pela reação.
Reações transfusionais
Anemia hemolítica autoimune
Anemia perniciosa
Doença hemolítica do feto e do recém-nascido
Púrpura trombocitopénica autoimune
Febre reumática aguda
Síndrome de Goodpasture
Doença de Graves
Miastenia gravis