Os polienos são uma classe de agentes fungicidas que englobam 2 fármacos com uso frequente na prática clínica, a nistatina e a anfotericina B. Ambos os fármacos atuam através da sua ligação ao ergosterol (um componente essencial das membranas das células fúngicas), criando poros na membrana, levando à saída de componentes intracelulares e, por conseguinte, à lise celular. Tanto a nistatina como a anfotericina B possuem um espectro amplo de atividade antifúngica, pouca ou nenhuma absorção oral e toxicidade significativa (sobretudo nefrotoxicidade) quando administradas por via parentérica. A nistatina é muito tóxica por via intravenosa; deste modo, é utilizada apenas no tratamento de infeções fúngicas da pele, membranas mucosas e lúmen GI. A anfotericina B é administrada por via intravenosa, intratecal ou intraperitoneal, ou inalatória, para tratar infeções fúngicas graves e com risco de vida. A resistência secundária à nistatina e à anfotericina B é rara, mas tem aumentado.
Última atualização: Apr 23, 2025
Os polienos são uma das classes originais de fármacos antifúngicos. Atualmente, são utilizados na prática clínica 2 polienos primários:
A nistatina e a anfotericina B possuem estruturas químicas muito semelhantes, incluindo:
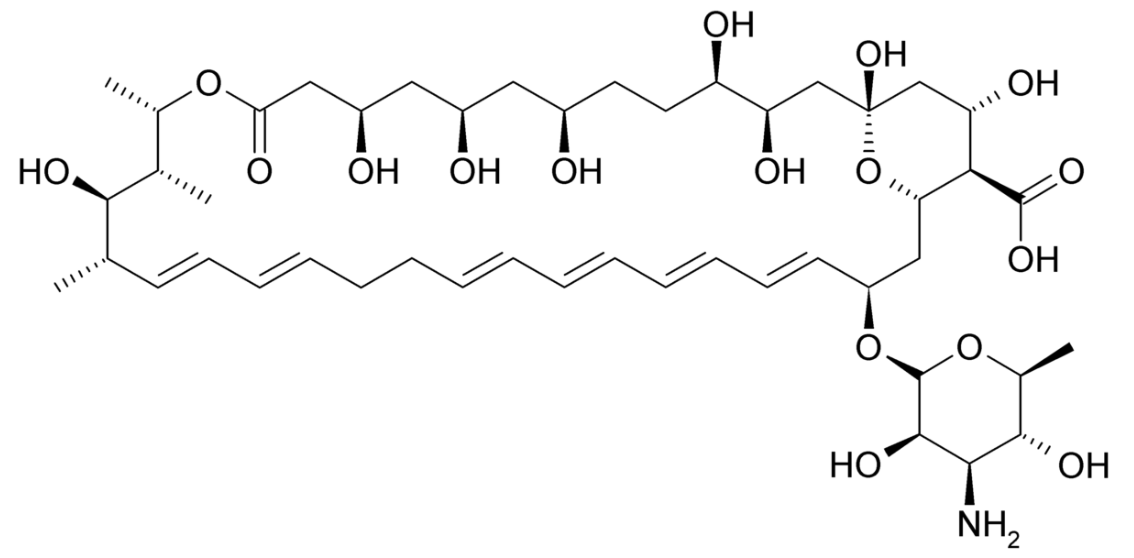
Estrutura química da nistatina
Imagem: “Nystatin” por Hoffmeier K. Licença: Domínio Público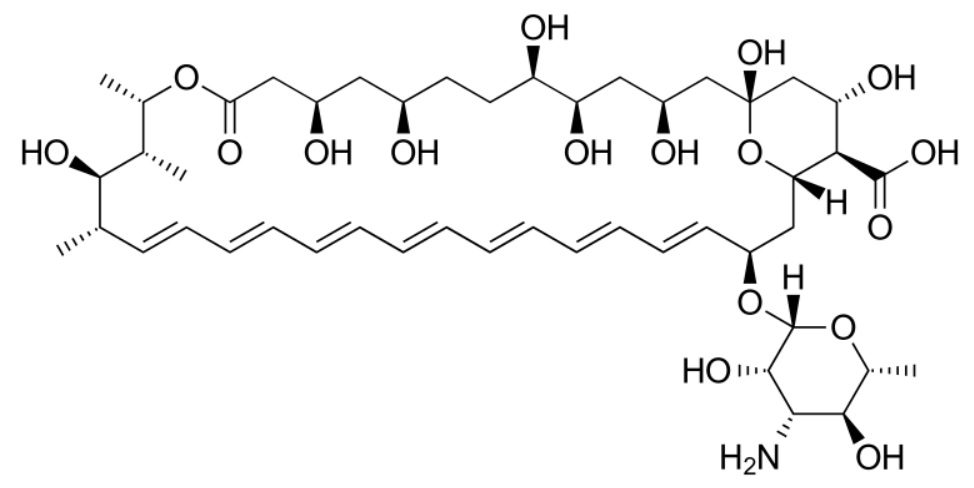
Estrutura química da anfotericina B
Imagem: “Amphotericin B” por The chemistds. Licença: Domínio PúblicoOs polienos criam esporos na membrana da célula fúngica através da ligação ao ergosterol; no entanto, o seu mecanismo de ação exato não está bem esclarecido.
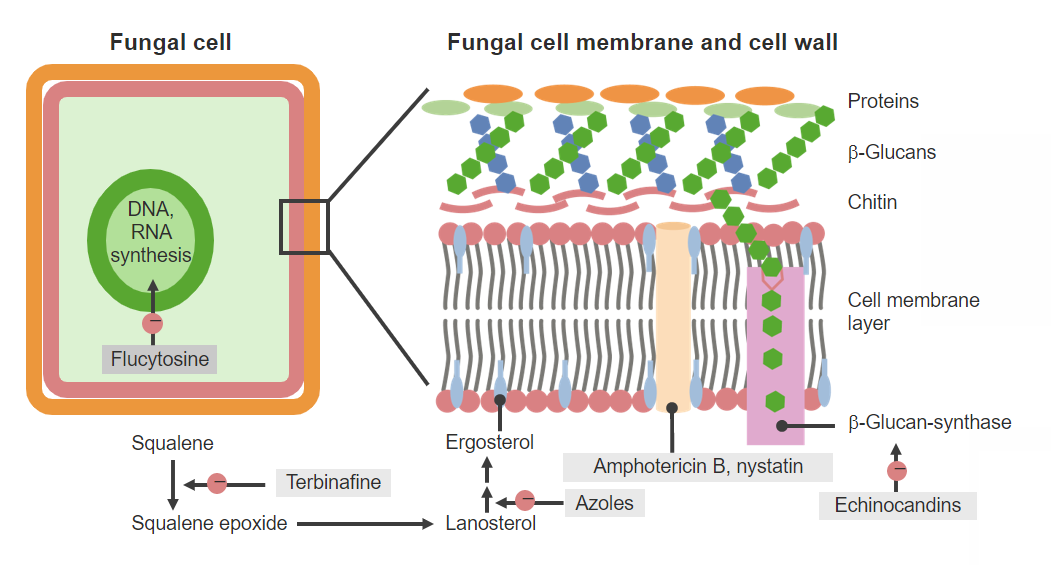
Agentes antifúngicos e mecanismos de ação
Imagem por Lecturio. Licença: CC BY-NC-SA 4.0A nistatina é utilizada apenas por via tópica e como suspensão oral (administrada com instruções para “bochechar e engolir”).
A nistatina está indicada em espécies de Candida suscetíveis que causam infeções fúngicas na(s):
Devido à sua toxicidade e à disponibilidade de agentes menos tóxicos, a anfotericina B deve ser ponderada apenas em indivíduos com infeções fúngicas invasivas graves, com risco de vida ou incapazes de tolerar agentes alternativos.
Espectro de atividade:
A anfotericina B é ativa contra:
Resistência:
Microorganismos com resistência intrínseca à anfotericina B:
A nistatina tópica e oral tem poucos efeitos adversos. A única contra-indicação é história prévia de reação alérgica.
A terapêutica com anfotericina B é frequentemente limitada pela sua toxicidade, associada a insuficiência renal induzida por fármacos. Os efeitos adversos podem ser divididos em reações imediatas relacionadas com a perfusão e efeitos devido à toxicidade cumulativa.
Toxicidade relacionada com a perfusão:
Toxicidade cumulativa:
Contra-indicações e precauções:
A resistência secundária à anfotericina B é rara, mas tem aumentado. Os principais mecanismos de resistência incluem:
| Classe de fármacos (exemplos) | Mecanismo de ação | Relevância clínica |
|---|---|---|
| Azóis (Fluconazol, Voriconazol) | Inibem a produção de ergosterol (componente importante da membrana celular fúngica), bloqueando a enzima lanosterol 14-α-desmetilase |
|
| Polienos (Anfotericina B, Nistatina) | Ligam-se ao ergosterol na membrana da célula fúngica e criam poros artificiais na membrana → saída de componentes celulares e lise celular (morte) consequente | Anfotericina B:
Nistatina:
|
| Equinocandinas (Caspofungina, Micafungina, Anidulafungina) | Inibem a β-glucano sintetase (enzima que sintetiza β-glucano, um componente estrutural importante da parede celular fúngica) → parede celular frágil → lise celular |
|
| Griseofulvina |
|
|
| Terbinafina | Inibe a enzima esqualeno epoxidase → bloqueia a produção de epóxido de esqualeno, um precursor do ergosterol e componente fundamental da membrana celular |
|
| Flucitosina | Análogo da pirimidina com metabolitos que:
|
|