As síndromes de neoplasia endócrina múltipla são doenças hereditárias autossómicas dominantes caracterizadas por 2 ou mais tumores produtores de hormonas envolvendo os órgãos do sistema endócrino. Existem diferentes tipos de MEN, nomeadamente a MEN1–4. A síndrome MEN1 está associada à mutação do gene MEN1 e implica uma predileção por hiperparatiroidismo primário, adenomas hipofisários (pituitários) e tumores pancreáticos (os 3 P's). Devida à mutação do proto-oncogene RET, a síndrome MEN2 pode ser posteriormente categorizada como MEN2A e MEN2B. O carcinoma medular da tiroide e o feocromocitoma são condições frequentes. A variante MEN2A está associada ao hiperparatiroidismo primário, enquanto a MEN2B (também considerada MEN3) se associa a neuromas e ao fenótipo marfanoide. A entidade mais recente e rara, MEN4, tem características da MEN1, mas resulta de mutações no CDKN1B. O diagnóstico é clínico e os tumores são detetados com base em exames de imagem e nos níveis das hormonas correlacionadas. Os testes genéticos desempenham um papel crucial nas síndromes MEN2 para determinar o tratamento posterior. O tratamento depende dos tumores presentes e da mutação genética.
Última atualização: May 4, 2022
As síndromes de neoplasia endócrina múltipla (MEN) são doenças genéticas caracterizadas pela presença de ≥ 2 tumores endócrinos.
| MEN1 | MEN2A e MEN2B | MEN4 | |
|---|---|---|---|
| Padrão | Autossómica dominante | Autossómica dominante | Autossómica dominante |
| Mutação genética | Gene MEN1 no cromossoma 11 (11q13) | Proto-oncogene RET no cromossoma 10 (10q11.2) | CDKN1B no cromossoma 12 (12p13) |
| Características clínicas |
|
MEN2A
MEN2B
|
|
| Tratamento |
|
|
|
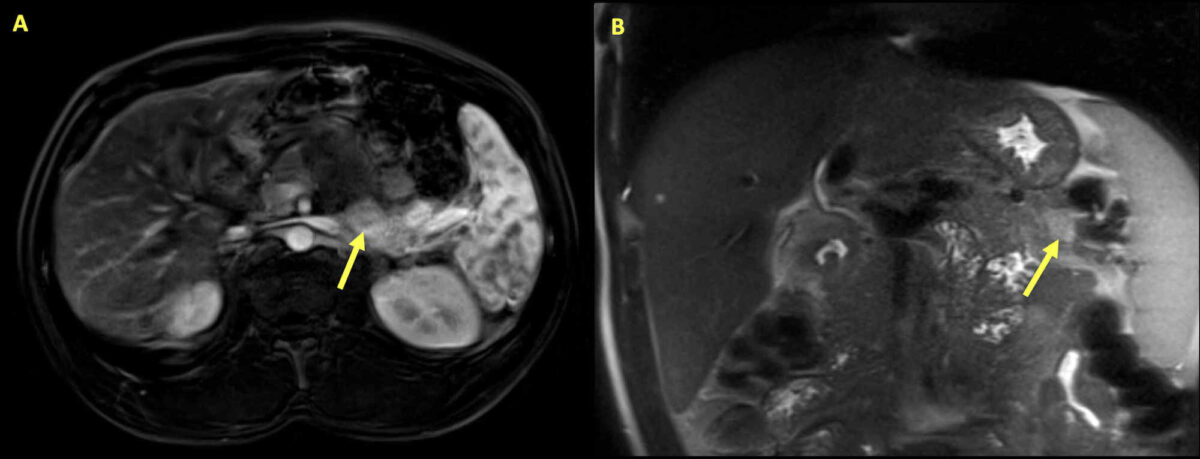
Insulinoma:
Ressonância magnética do abdómen de um homem de 34 anos que se apresentou com hipoglicemia e hipercalcémia. Veem-se múltiplas lesões pancreáticas, com as setas a destacar a maior lesão. A massa é uma área de 2,8 cm x 1,3 cm no pâncreas, de realce variável e restrição à difusão, consistente com um insulinoma.
As análises posteriores revelaram níveis elevados de paratormona (PTH) intacta. Com hiperparatiroidismo primário e insulinoma, foi realizado o teste genético, que mostrou mutação no gene MEN1, o que confirmou a presença da síndrome MEN1.
No sentido de recordar os locais de desenvolvimento de tumores na MEN1, lembrar os 3 Ps:
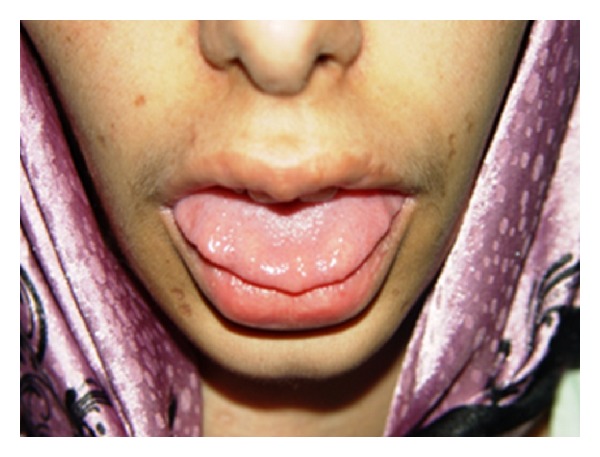
Neoplasia endócrina múltipla (MEN) 2B:
A imagem mostra neuromas no terço anterior da língua num doente com MEN2B
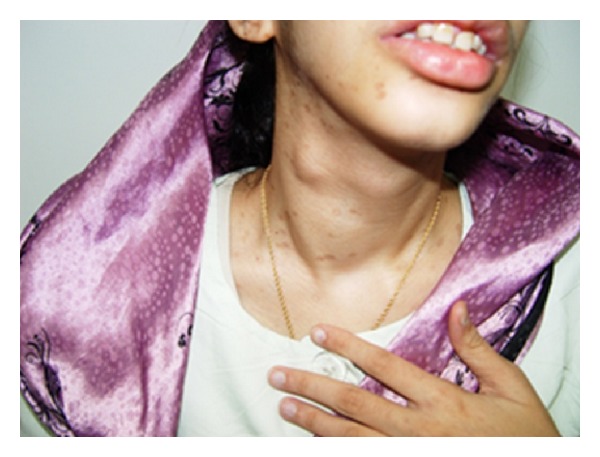
Neoplasia endócrina múltipla (MEN) 2B:
O doente da imagem apresenta um bócio com um nódulo da tiroide no lobo direito. A biópsia revelou posteriormente um carcinoma medular da tiroide.
No sentido de recordar os locais de desenvolvimento de tumores na MEN2, lembrar os 3Ps: