Os corpos cetónicos são uma importante fonte de energia e o seu metabolismo é um processo fortemente regulado. Quando as reservas de glucose Glucose A primary source of energy for living organisms. It is naturally occurring and is found in fruits and other parts of plants in its free state. It is used therapeutically in fluid and nutrient replacement. Lactose Intolerance no corpo diminuem, mais MAIS Androgen Insensitivity Syndrome ácidos gordos são disponibilizados ao fígado para oxidação, levando à consequente produção de moléculas ricas em energia, sobretudo acetil-CoA. O acetil-CoA pode entrar no ciclo do ácido cítrico no fígado ou ser utilizado para a síntese de corpos cetónicos. Estes, posteriormente, podem viajar através do sangue por todo o corpo. As células (sobretudo no músculo esquelético e no cérebro) conseguem converter os corpos cetónicos de volta para acetil-CoA, que consegue assim entrar no ciclo do ácido cítrico e produzir ATP. Os corpos cetónicos constituem uma forma do corpo utilizar a energia armazenada na gordura quando a glucose Glucose A primary source of energy for living organisms. It is naturally occurring and is found in fruits and other parts of plants in its free state. It is used therapeutically in fluid and nutrient replacement. Lactose Intolerance está indisponível ou a sua utilização é impossível.
Last updated: Apr 17, 2025
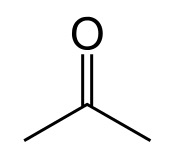
Acetona, um corpo cetónico
Imagem: “Skeletal formula of acetone” de Fvasconcellos. Licença: Domínio Público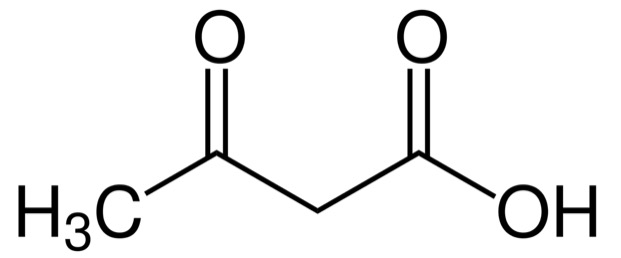
Ácido acetoacético, um corpo cetónico
Imagem: “Acetoacetic acid” de Jü. Licença: Domínio Público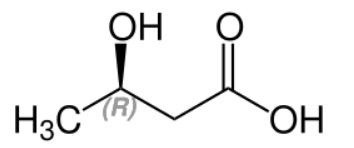
β-hidroxibutirato, um corpo cetónico
Imagem: “Strukturformel von (R)-3-Hydroxybuttersäure” de Jü. Licença: Domínio PúblicoA cetogénese é o processo de formação de corpos cetónicos, que ocorre nas mitocôndrias dos hepatócitos.
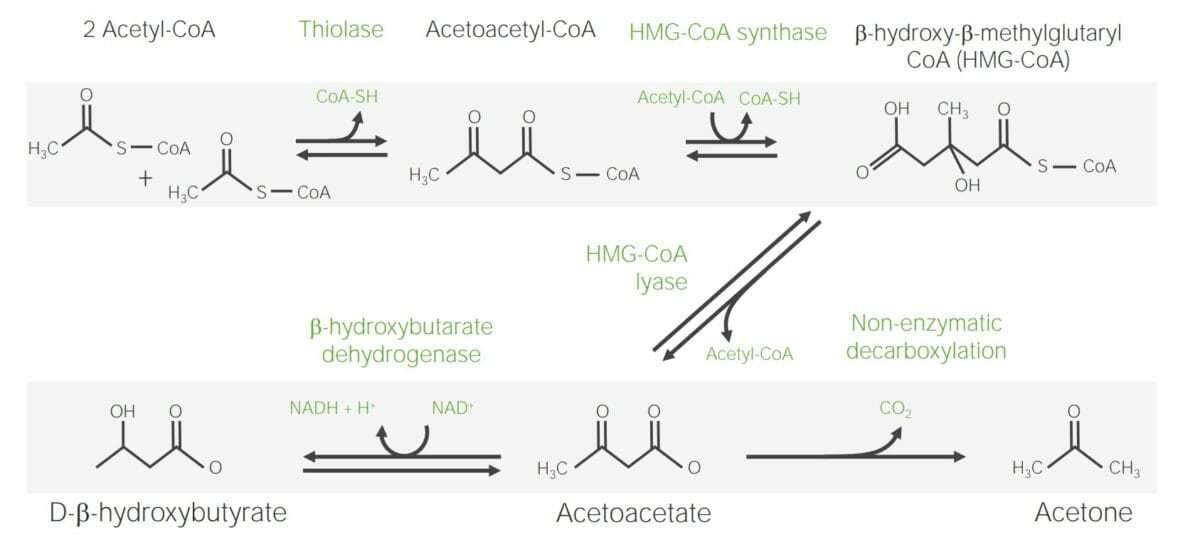
Etapas necessárias para a síntese de corpos cetónicos
Imagem de Lecturio.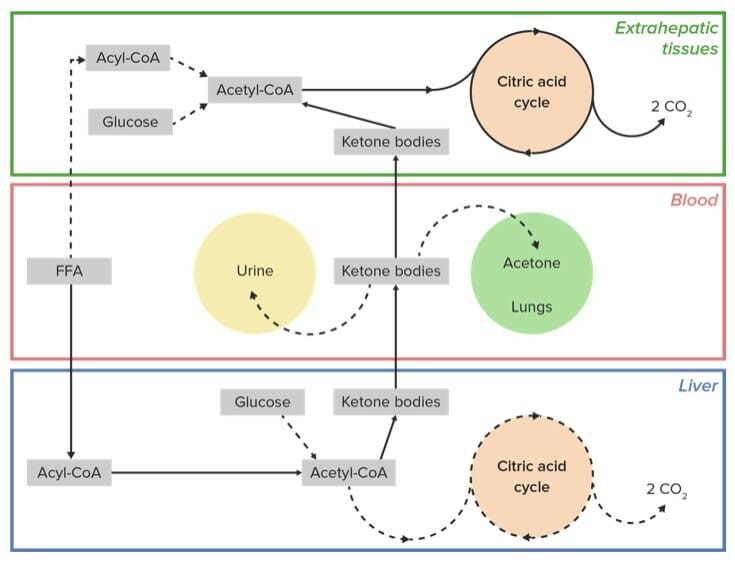
Ciclo do ácido cítrico:
Os ácidos gordos livres (AGL) são transportados até ao fígado (e alguns locais extra-hepáticos), onde são ativados em cadeias lipídicas de acil-CoA e, de seguida, metabolizados via β-oxidação em moléculas individuais de acetil-CoA. Quando a glucose é limitada, o acetil-CoA é convertido em corpos cetónicos. O acetoacetato e o β-hidroxibutirato viajam pelo sangue até aos tecidos extra-hepáticos onde são necessários (ex, músculo, cérebro) e convertidos de volta em acetil-CoA, que entra, posteriormente, no ciclo do ácido cítrico para gerar energia sob a forma de ATP. Algum do acetoacetato sofre uma conversão não enzimática em acetona, outro corpo cetónico, que entra no sangue e é exalado pelos pulmões. Outros corpos cetónicos são excretados pela urina antes de chegar aos seus tecidos extra-hepáticos alvo.
FFA (AGL): ácidos gordos livres
Linha sólida: via principal
Linha tracejada: Vias minor