Existem 2 componentes principais nas glândulas suprarrenais, a medula e córtex. Cada um destes componentes secreta hormonas diferentes e apresenta mecanismos de regulação diferentes. A medula adrenal é a porção interna da glândula, e é responsável pela secreção de epinefrina e, em menor grau, norepinefrina. Estas hormonas funcionam em conjunto com o sistema nervoso simpático e contribuem para a resposta de luta ou fuga. O córtex adrenal é a porção externa da glândula e faz parte do eixo hipotálamo-hipófise-suprarrenal. O córtex é responsável pela secreção de mineralocorticoides, glucocorticoides e androgénios. A aldosterona (mineralocorticoide) está sobretudo envolvida na regulação do potássio e do volume de fluidos. Os glicocorticoides (por exemplo, cortisol) fornecem energia imediata ao organismo e têm propriedades anti-inflamatórias. Os andrógenos estimulam os caracteres sexuais secundários.
Última atualização: Jun 28, 2022
As glândulas suprarrenais têm 2 componentes principais com diferentes funções e mecanismos regulatórios.
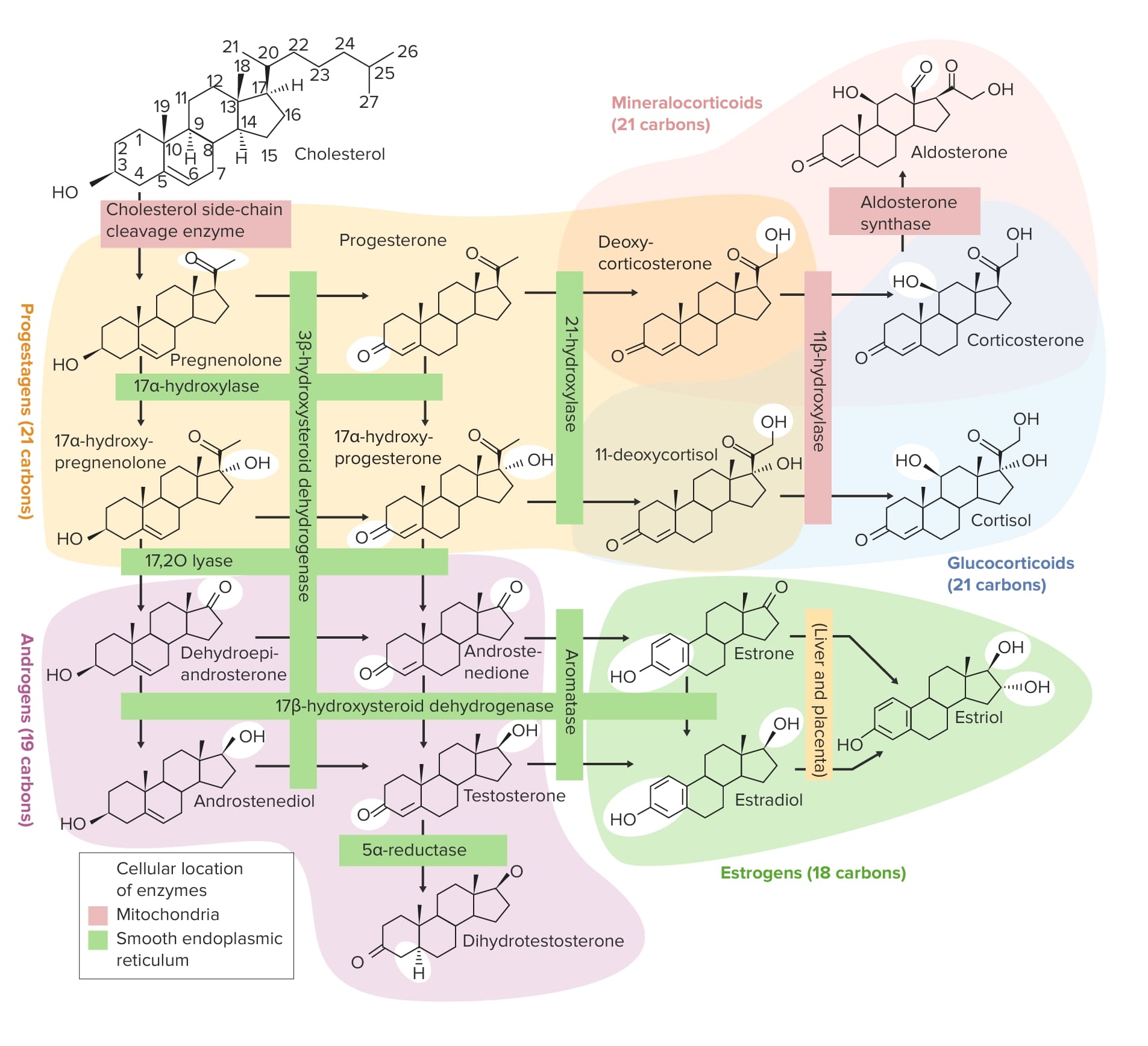
Visão geral das vias de esteroidogéneses
HSD: hidroxiesteroide desidrogenase
Hormonas secretada pelo córtex adrenal (e não pela medula) ajudam a regular e são controladas pelo eixo HPA.
O SRAA é um dos principais reguladores da pressão arterial, da água corporal total, dos níveis séricos de sódio e do equilíbrio do pH no organismo.
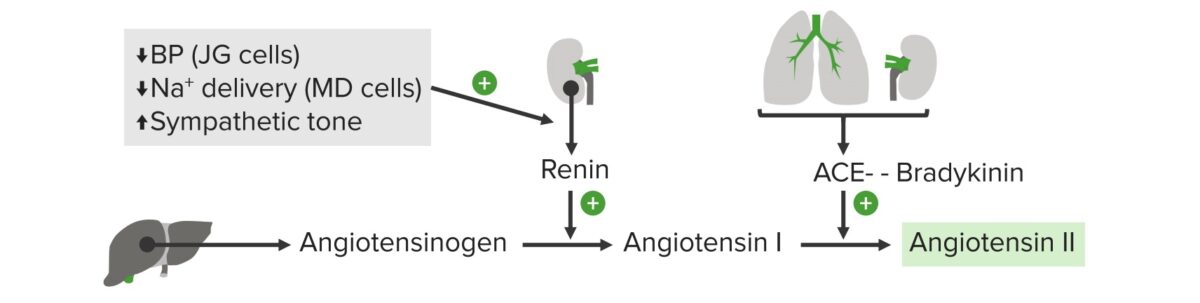
Diagrama do sistema renina-angiotensina-aldosterona:
O angiotensinogénio é secretado pelos hepatócitos. A renina é secretada pelas células justaglomerulares (JG) renais e converte o angiotensinogénio em angiotensina I. A secreção de renina é estimulada: pela diminuição da pressão arterial (PA), notada pelas células JG renais; pela diminuição do aporte de sódio ao rim, notado pelas células da mácula densa (MD); e pelo aumento do tónus simpático. A enzima conversora da angiotensina é secretada pelos pulmões e converte a angiotensina I em angiotensina II.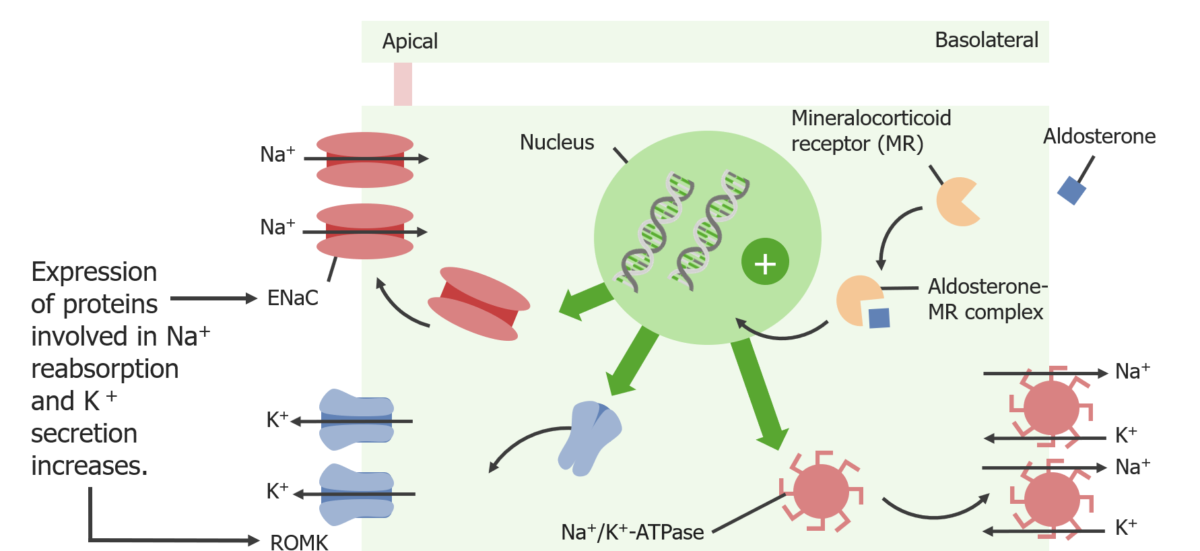
Ações de aldosterona na célula principal: A aldosterona estimula a produção dos canais epiteliais de sódio (ENaC), canais renais medulares externos de potássio (ROMK) e Na + / K+ ATPase. A Na + / K+ ATPase cria um gradiente químico de Na + (permitindo um aumento da reabsorção de Na + através dos ENaCs) e um gradiente químico para o K+ (permitindo uma secreção aumentada de K+ através dos canais ROMK)
ENaC: canal epitelial de sódio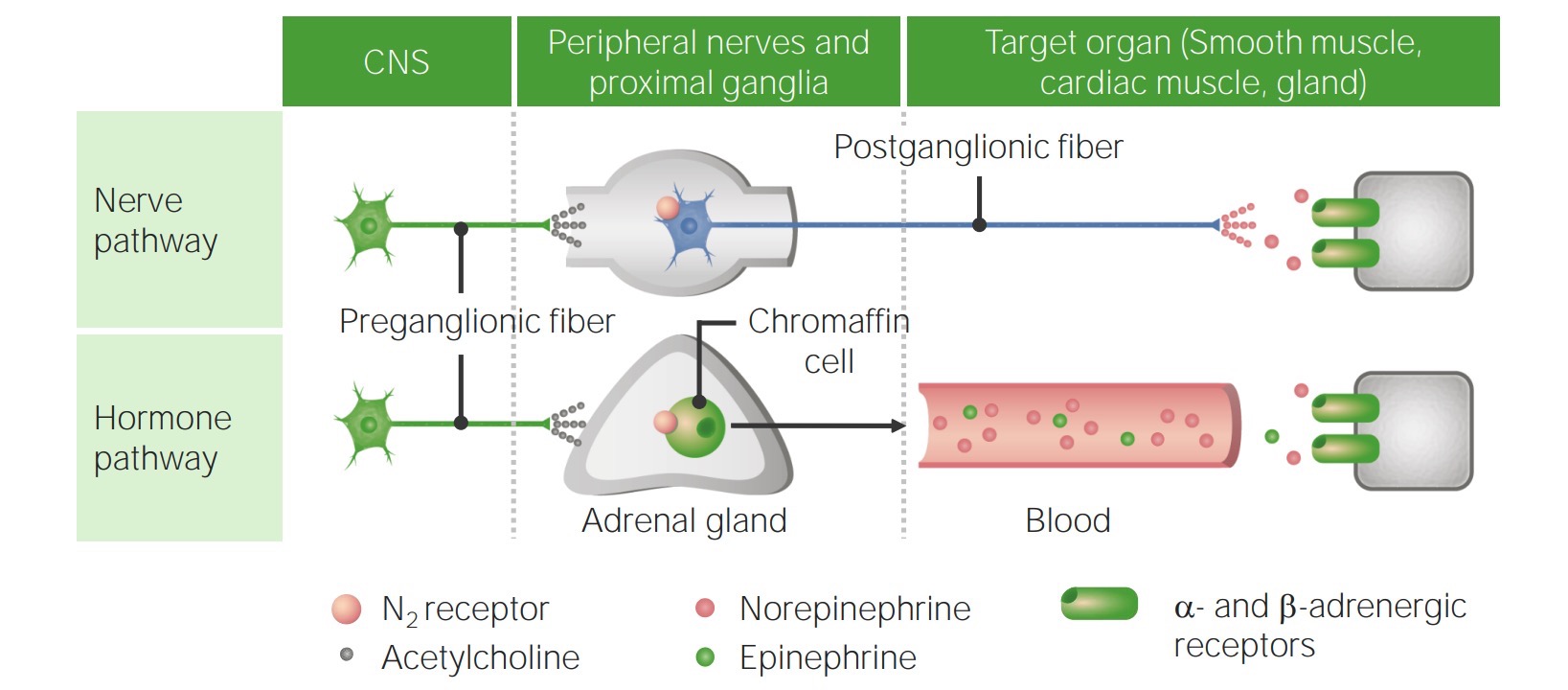
Diferenças entre as vias nervosas e hormonais utilizadas para a sinalização simpática:
A medula adrenal é considerada um gânglio simpático modificado porque secreta catecolaminas tal como os nervos pós-ganglionares do sistema nervoso simpático. As células cromafim da medula adrenal são únicas, devido à sua capacidade de converter estímulos nervosos em sinais endócrinos.
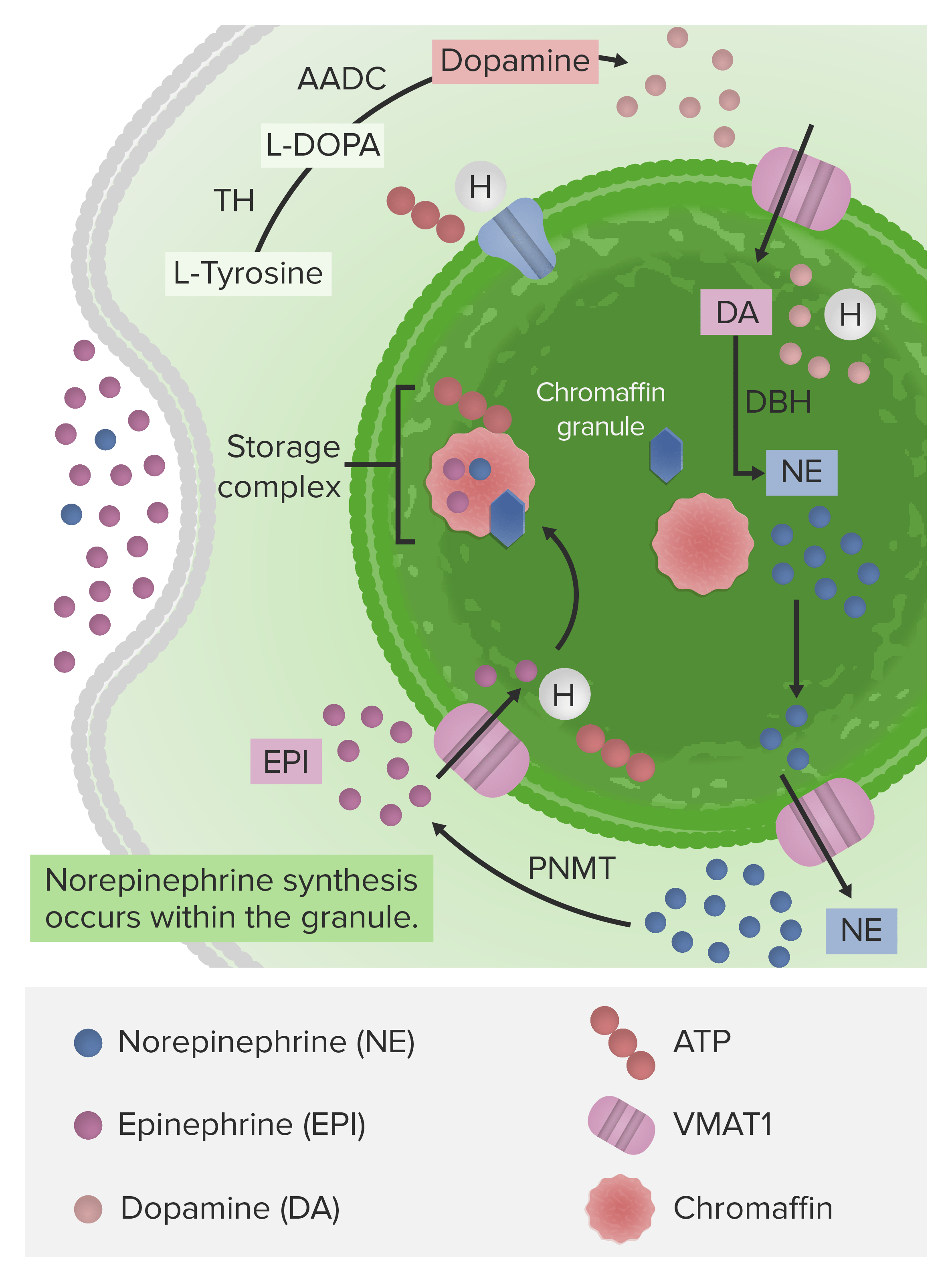
A via sintética da norepinefrina (NE) e epinefrina (E) a partir da dopamina (sintetizada a partir do aminoácido L-tirosina):
Note que a dopamina é convertida em norepinefrina nos grânulos cromafins (onde se localiza a enzima sintética). A enzima que converte a norepinefrina em epinefrina licaliza-se no citosol. A epinefrina então move-se de volta aos grânulos cromafins e é armazenada até que seja recebido um sinal do sistema nervoso simpático que promova a sua libertação.
TH: tirosina hidroxilase
L-DOPA: levo-diidroxifenilalanina
AADC: descarboxilase de L-aminoácidos aromáticos
DBH: dopamina β-hidroxilase
PNMT: feniletanolamina N-metiltransferase
VMAT1: transportador vesicular de monoamina 1
O principal objetivo das catecolaminas medulares é complementar os efeitos do sistema nervoso simpático. Visto que estas substâncias são libertadas diretamente na corrente sanguínea como hormonas, os seus efeitos duram mais tempo do que quando as catecolaminas são libertadas como neurotransmissores. Estes efeitos incluem características da resposta de luta ou fuga:
Existem várias condições clínicas que resultam de alterações nas hormonas adrenais. Algumas das condições mais importantes em termos clínicos incluem: