A hemocromatose hereditária (HH) é uma doença autossómica recessiva mais frequentemente associada a mutações no gene HFE. Os pacientes apresentam aumento da absorção intestinal de ferro e deposição de ferro em vários órgãos, como fígado, coração, pele e pâncreas. A apresentação clínica inclui a tríade de cirrose, diabetes e pele bronzeada. Outros achados dependem do(s) órgão(s) envolvido(s). O diagnóstico consiste em estudos do ferro, que mostram elevação de transferrina (Tf) e ferritina. O estudo genético é recomendada entre os membros da família. Estudos de imagem e invasivos são realizados dependendo das complicações associadas. O tratamento requer flebotomia (ou terapia com quelantes de ferro em alguns casos) para prevenir a progressão da doença. O prognóstico é bom para pacientes que estão no início da doença e em tratamento. A presença de fibrose hepática é um fator de mau prognóstico.
Última atualização: Jan 17, 2024
A hemocromatose hereditária (HH) é:
É importante notar que as causas da sobrecarga de ferro podem sobrepor-se ou ocorrer em simultâneo.
Distúrbios secundários de sobrecarga de ferro (adquiridos):
Certas condições requerem uma diminuição ou aumento na absorção de ferro e ferro circulante, uma via regulada pela hepcidina :
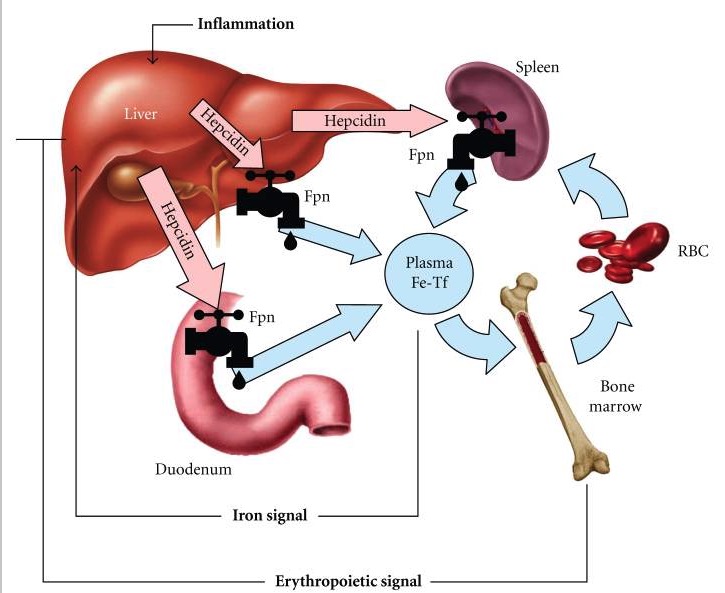
A interação hepcidina-Fpn determina o fluxo de ferro para o sangue.
1. O ferro da dieta sofre absorção intestinal no duodeno.
2. O ferro move-se do duodeno através do exportador de ferro, Fpn, e entra na circulação via Tf.
3. A transferrina fornece o ferro à medula óssea para a síntese de hemoglobina.
4. À medida que os eritrócitos envelhecem são fagocitadas por macrófagos (baço), liberando ferro novamente na circulação através de Fpn.
5. Quando há aumento de ferro ou inflamação, a hepcidina derivada do fígado aumenta, que reduz a absorção duodenal de ferro e o ferro de libertação da degradação de eritrócitos senescentes.
6. Quando há necessidade de sintese de GV, a eritropoietina inibe a hepcidina para permitir maior absorção de ferro (do intestino) e liberar ferro dos macrófagos com eritrócitos senescentes.
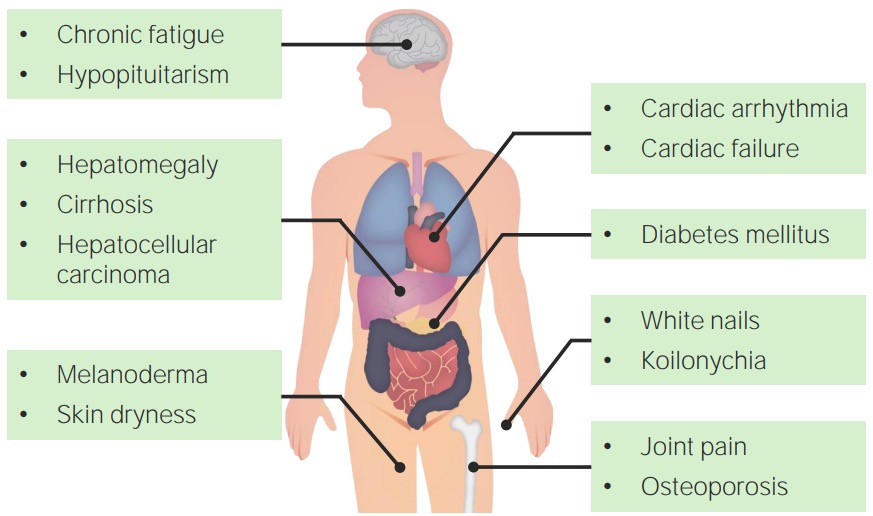
Características clínicas da hemocromatose
Imagem por Lecturio.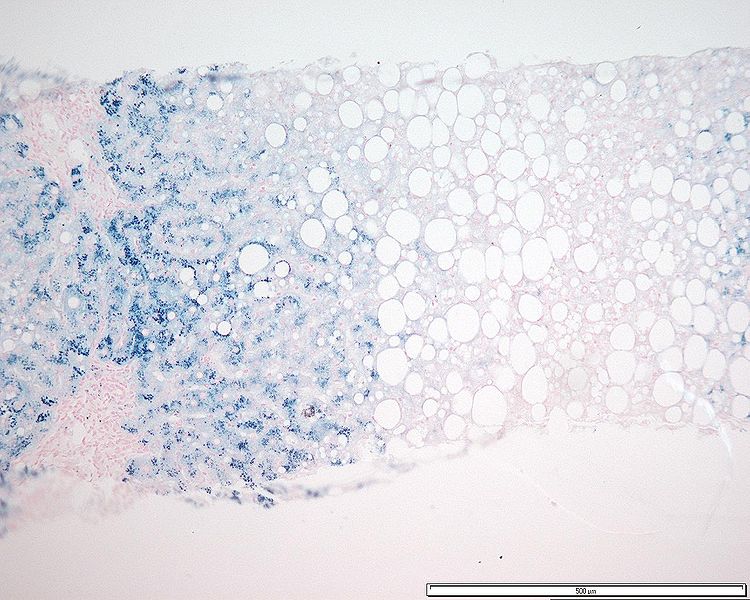
Acumulação de ferro nos hepatócitos em paciente com hemocromatose (corado com azul da Prússia)
Imagem: “Grade 3 hepatocyte iron accumulation” por Mathew, J. et al. Licença: CC BY 3.0.