Os estados de hipercoagulabilidade (também chamados de trombofilias) são um grupo de doenças hematológicas definidas por um risco aumentado de formação de coágulos (isto é, trombose) devido a um aumento de pró-coagulantes, uma diminuição de anticoagulantes ou uma diminuição da fibrinólise. Existem causas hereditárias e adquiridas, sendo o fator V de Leiden a causa hereditária mais comum. Clinicamente, os estados de hipercoagulabilidade apresentam eventos trombóticos, que causam oclusão dos vasos e podem levar a danos nos órgãos. Os distúrbios trombóticos podem ser fatais se não forem tratados, e o tratamento geralmente envolve anticoagulantes.
Última atualização: Jan 17, 2024
A hipercoagulabilidade, também conhecida como trombofilia, refere-se ao aumento da tendência do sangue para formar coágulos, conhecidos como trombos. Os estados de hipercoagulabilidade podem ser herdados ou adquiridos.
Prevalência de trombofilias hereditárias:
| Alteração | Prevalência | Risco de TEV |
|---|---|---|
| Fator V de Leiden | 3%–7% | 4.3% |
| Mutação de protrombina G20210A | 1%–3% | 1.9% |
| Deficiência de proteína C (heterozigótico) | 0,02%–0.05% | 11.3% |
| Deficiência de proteína S (heterozigótico) | 0.01% | 32.4% |
| Deficiência de antitrombina | 0,02 %–0.04% | 17.5% |
Estados de hipercoagulabilidade adquiridos mais comuns:
Impacto clínico:
Os eventos trombóticos ocorrem sob 3 condições primárias, que compõem a tríade de Virchow. Essas 3 condições são:
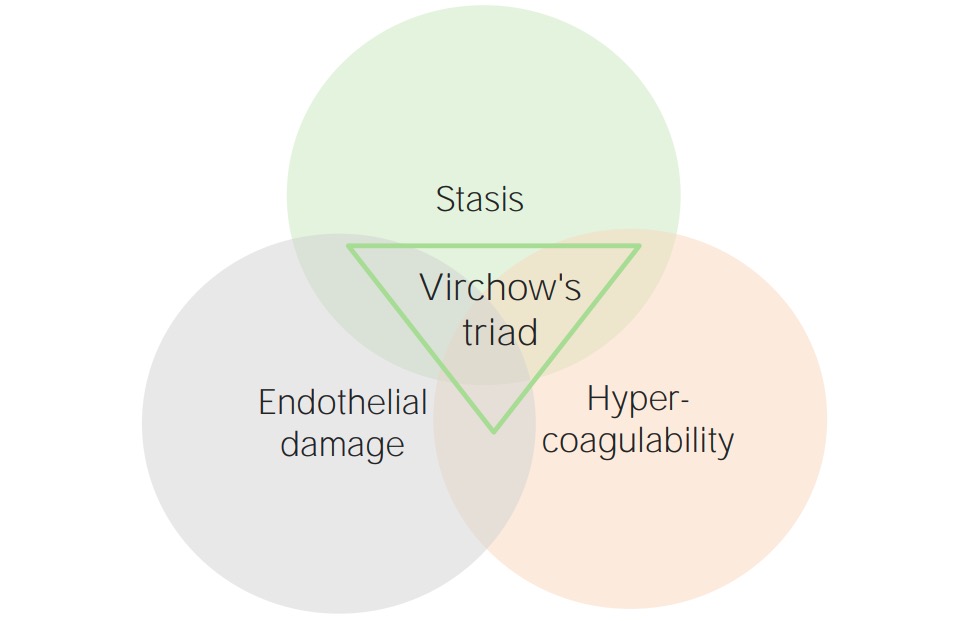
Tríade de Virchow
Imagem por Lecturio.Os estados de hipercoagulabilidade podem ser primários (hereditários) ou secundários (adquiridos).
| Alteração | Padrão de transmissão | Fisiopatologia |
|---|---|---|
| Fator V de Leiden | Autossómico dominante com penetrância incompleta |
|
| Protrombina G20210A (também conhecida como mutação do fator II) | Autossómica recessiva |
|
| Deficiência de antitrombina | Autossómica dominante |
|
| Deficiência de proteína C ou S | Autossómica dominante (rara; pode ser recessiva) |
|
| Síndrome das plaquetas viscosas (“Sticky platelet syndrome”) | Autossómica dominante |
|
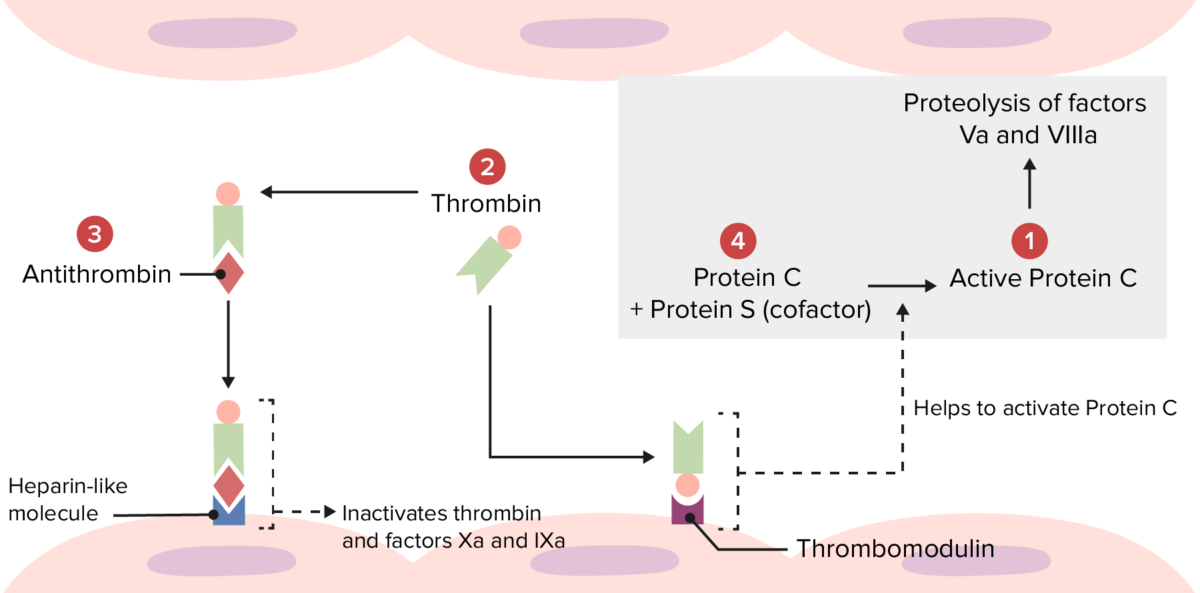
Visão geral da via trombolítica fisiológica:
Vários distúrbios de hipercoagulabilidade ocorrem devido a anomalias nos seguintes locais.
Mutações em 1: Fator V de Leiden torna o fator Va resistente à degradação pela proteína C ativada.
Mutações em 2: A mutação da protrombina produz uma quantidade aumentada de protrombina, levando à formação excessiva de trombina.
Mutações em 3: A deficiência de antitrombina leva à redução da inativação da trombina e dos fatores Xa e IXa.
Mutações em 4: A deficiência de proteína C ou S leva à inativação reduzida dos fatores Va e VIIIa.
Muitas outras condições e estados aumentam o risco trombótico ao afetar os componentes da tríade de Virchow (tipicamente, estase, lesão endotelial ou ambos) de forma a promover a trombose. Estas condições incluem:
A apresentação clínica primária de um estado de hipercoagulabilidade será um evento trombótico ou um familiar assintomático de um paciente com uma doença de hipercoagulabilidade primária conhecida que se apresente para uma avaliação.
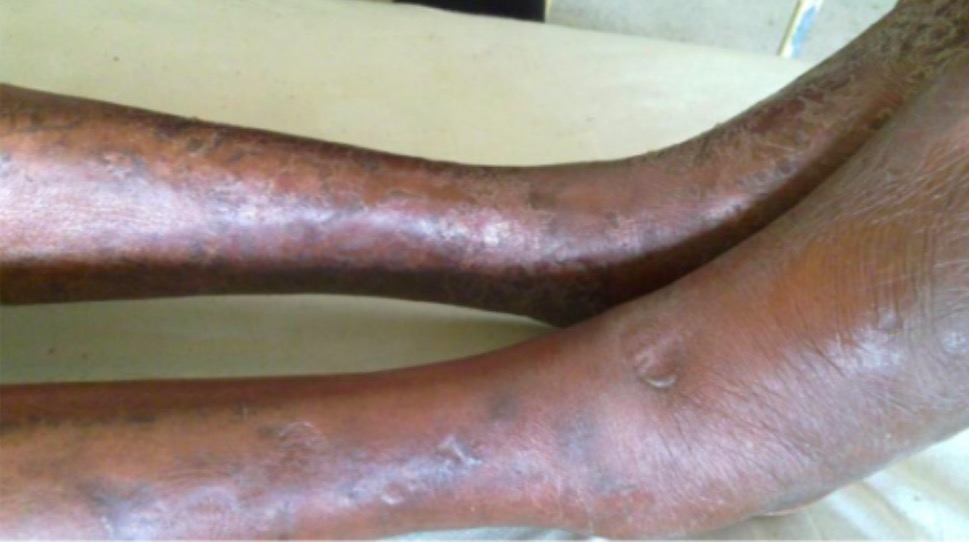
Edema depressível com aumento do diâmetro da perna direita devido a uma trombose venosa profunda
Imagem : “Pitting edema of right leg” por Department of medicine (ward 45), the National hospital of Sri Lanka, (Regent Street), Colombo, (00800), Sri Lanka Licença: CC BY 2.0As mutações do fator V de Leiden e da protrombina G20210A não têm apresentações únicas além de eventos trombóticos recorrentes. Vários achados específicos podem ser observados em:
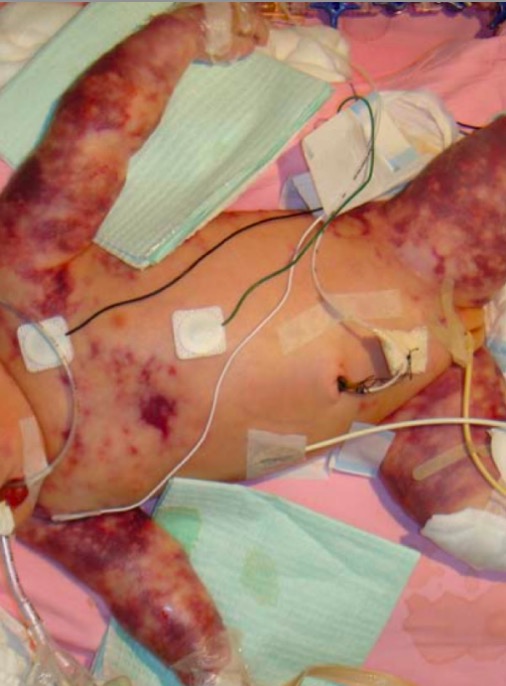
Púrpura fulminante neonatal
Imagem : “Purupura fulminans” por Department of Paediatrics, The Chinese University of Hong Kong, Prince of Wales Hospital, Shatin, Hong Kong.Licença: CC BY 2.0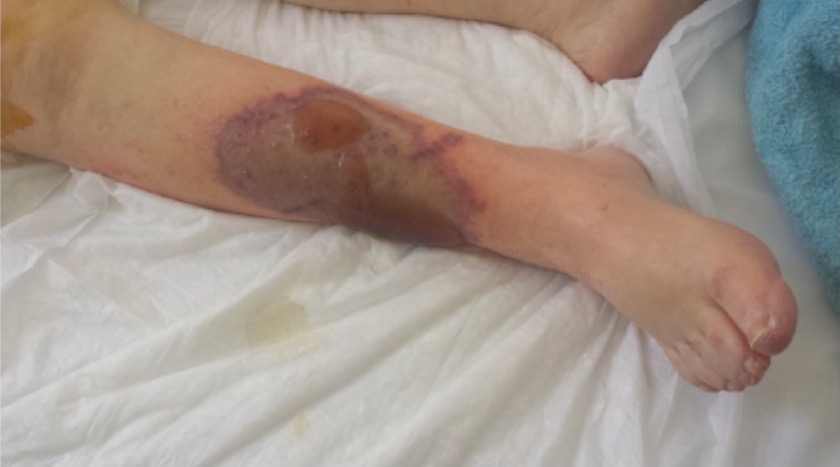
Necrose cutânea induzida por varfarina
Imagem : “Patient’s right leg” por 1st Department of Surgery, Vascular Surgery Unit, Laikon General Hospital, Medical School of Athens, Agiou Thoma 17, 11527 Athens, Greece.. Licença: CC BY 4.0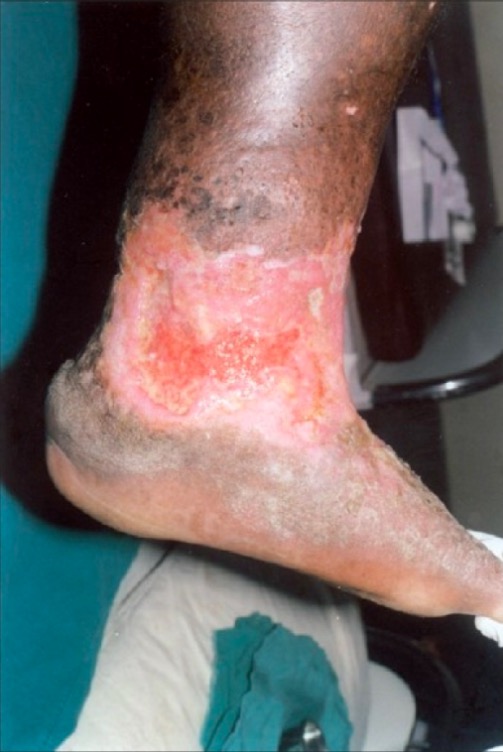
Úlcera de estase venosa irregular e não cicatrizada na parte inferior da perna e no tornozelo, com tecido de granulação não saudável:
Há também lipodermatoesclerose circundante, dermatite de estase e pigmentação acastanhada da pele, todas características de insuficiência venosa crónica.
Estes estudos devem ser realizados na maioria dos pacientes com suspeita de eventos trombóticos.
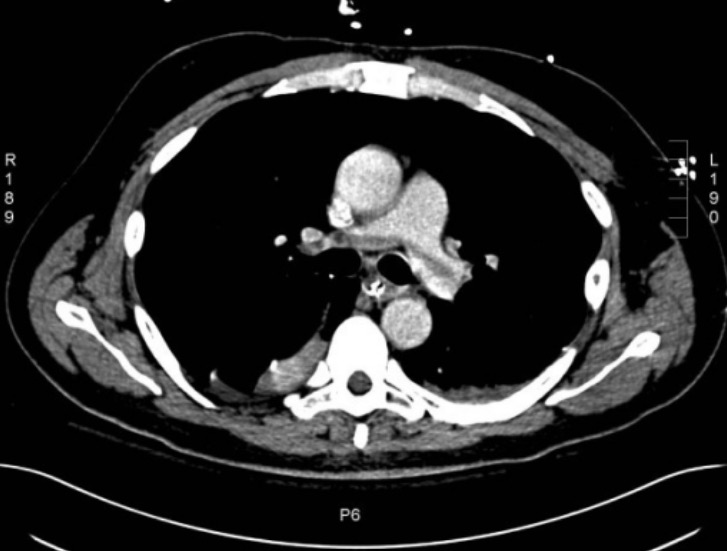
Angiografia de TC do tórax mostrando um êmbolo pulmonar em sela
Imagem: “Large saddle pulmonary embolism” por Rhode Island Hospital, Brown University School of Medicine, 2 Dudley Street, Providence, RI, USA. Licença: CC BY 2.0Considerar solicitar exames específicos adicionais para rastreio de uma trombofilia hereditária se os pacientes cumprirem qualquer um dos seguintes critérios:
Se os pacientes cumprirem qualquer um dos critérios acima para iniciar uma investigação de trombofilia, podem ser solicitados os seguintes exames para rastrear trombofilias hereditárias específicas:
Nota: A trombose aguda e/ou os anticoagulantes podem reduzir as concentrações plasmáticas de antitrombina, de proteína C e de proteína S.
Em pacientes com trombofilias hereditárias conhecidas ou que tenham fatores de risco para trombose:
A anticoagulação é a base da terapia para eventos trombóticos. As opções para anticoagulação inicial incluem:
Duração da terapia: