A degenerescência macular ligada à idade (DMLI) é uma doença visual que ocorre por alterações na mácula, a área responsável pela visão de alta acuidade. É caracterizada pela perda central de visão com visão periférica relativamente mantida. Os fatores de risco incluem a idade avançada, o tabagismo, história familiar e doenças cardiovasculares. Há dois tipos principais de DMI: a exsudativa (húmida) e a não exsudativa (seca). A diferença entre estes 2 tipos é a presença de neovascularização na coroide na DMI húmida, o que se manifesta como distorção ou perda visual. A DMI seca, que ocorre com maior frequência, é geralmente assintomática, mas numa minoria dos casos pode levar à perda da visão. Não há tratamento para a DMI seca precoce, mas a suplementação que resultou do estudo AREDS 2 (Age-Related Eye Disease Study 2) esta recomendada em caso de doença avançada. Inibidores do fator de crescimento endotelial vascular são utilizados na DMI húmida.
Última atualização: Jul 6, 2022
Degenerescência macular ligada à idade (DRI):
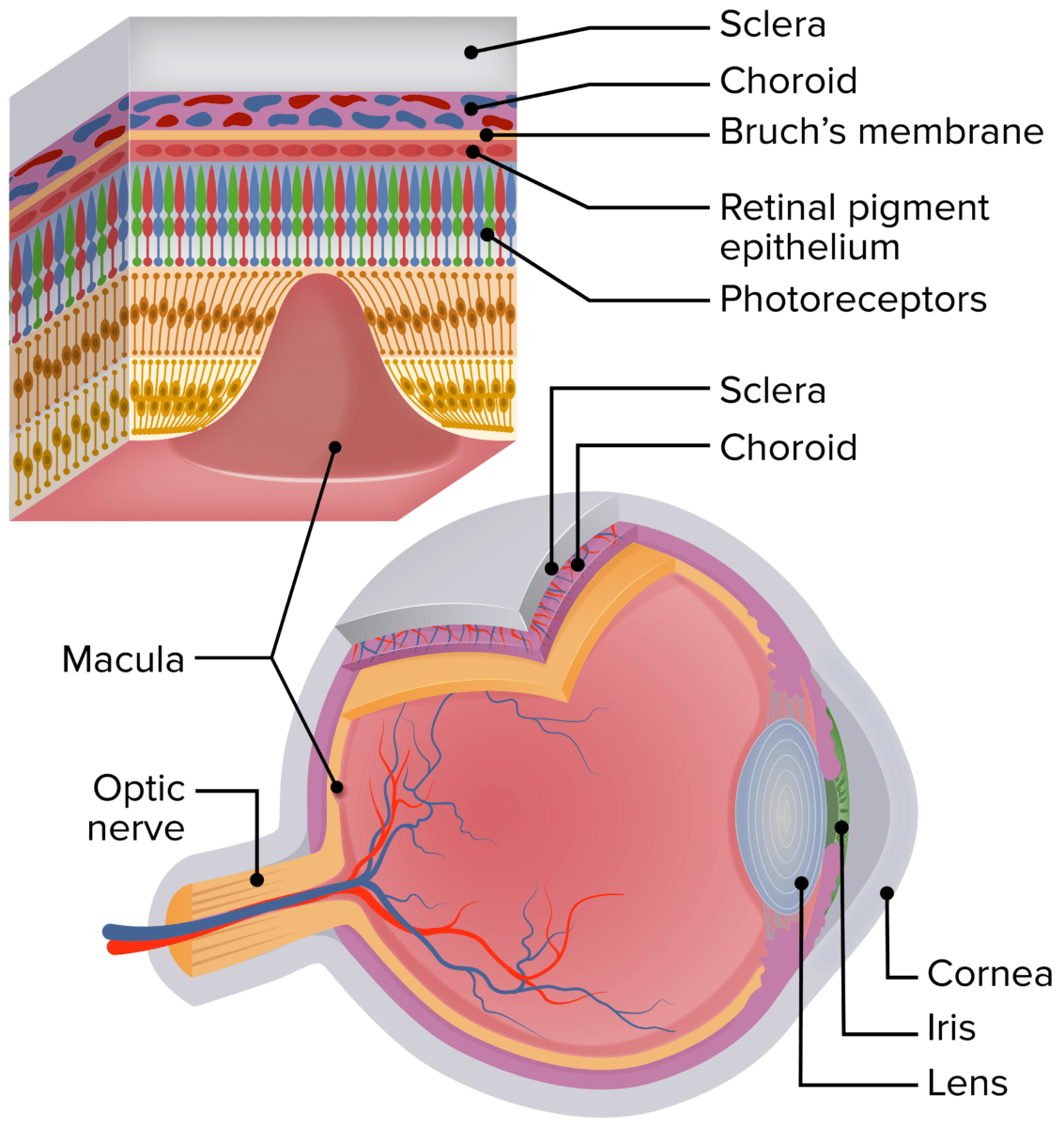
Esquema do olho humano mostrando a localização da mácula. A secção ampliada da retina mostra as camadas da retina e a relação dos fotorreceptores com o EPR, a membrana de Bruch e a camada coriocapilar.
Image by Lecturio.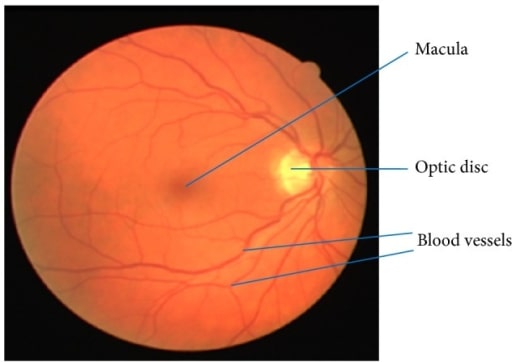
Imagem da retina onde se pode visualizar a mácula, os vasos sanguíneos e o disco ótico
Imagem: “Retinal image showing blood vessels and OD” por Department of ECE, SACS MAVMM Engineering College, Madurai, Tamil Nadu 625 301, India. Licença: CC BY 3.0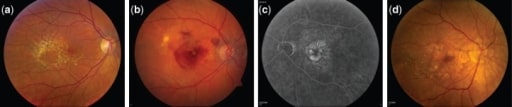
Fotografias do fundo que mostra diferentes estadios de progressão da DMI.
(a) Drusa grande e intermedia no estadio intermedio da DMI
(b) DMI neovascular: olho direito com fluido subretinal, hemorragia e exsudado duro na presença de neovascularização da coroide
(c) Angiografia de fluoresceína num caso de DMI neovascular: o olho esquerdo mostra hiperfluorescência o que corresponde à área de neovascularização da coroide
(d) Atrofia geográfica central: olho direito com evidência de atrofia geográfica envolvendo o centro da fóvea com evidência de uma drusa grande temporalmente
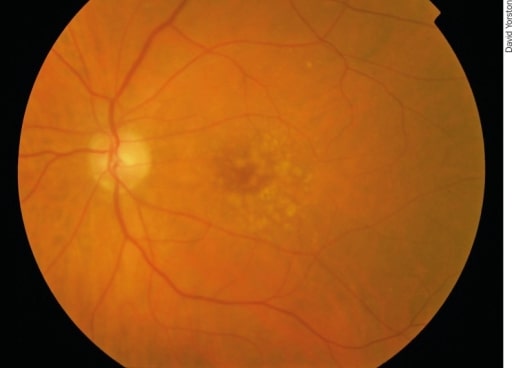
DMI precoce: existem pontos irregulares pálidos na mácula, chamadas drusas. São causadas por uma acumulação de produtos resultantes do metabolismo dos fotorreceptores. Embora as drusas estejam associados à DMI, a maioria dos doentes com drusas não desenvolve DMI grave.
Imagem: “Early AMD” por Africa Regional Medical Advisor: Fred Hollows Foundation, Kigali, Rwanda. Licença: CC BY 2.0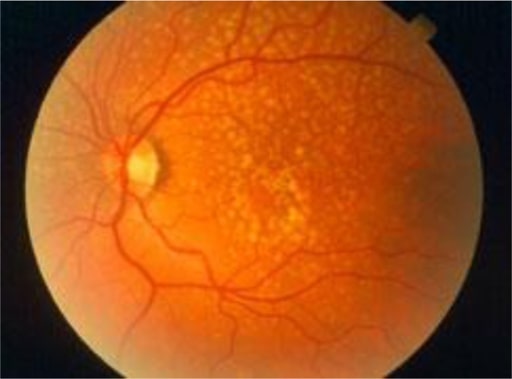
As drusas são depósitos amarelados que se situam debaixo da retina, o tecido sensível à luz na parte de trás do olho. As drusas consistem em lípidos e proteínas de gordura.
Imagem: “Oxidative stress, innate immunity, and age-related macular degeneration” por Department of Ophthalmology and Shiley Eye Institute, University of California San Diego, San Diego, CA, USA. Licença: CC BY 4.0
Exemplo de visão normal
Imagem: “An example of normal vision” por National Eye Institute. License: Public Domain
Visão afetada pela DMI
Imagem: “The same view with age-related macular degeneration” por National Eye Institute. Licença: Public Domain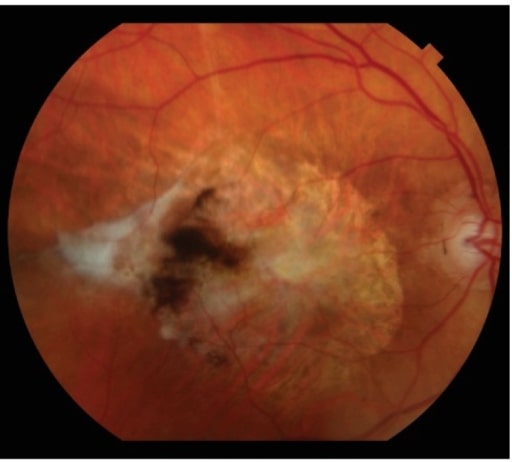
A cicatriz fibrótica subretinal é a manifestação da fase terminal da DMI neovascular.
Imagem: “Subretinal fibrotic scarring” por Retina Service, Department of Ophthalmology, Massachusetts Eye and Ear Infirmary, Harvard Medical School, Boston, MA 02114, USA. Licença: CC BY 4.0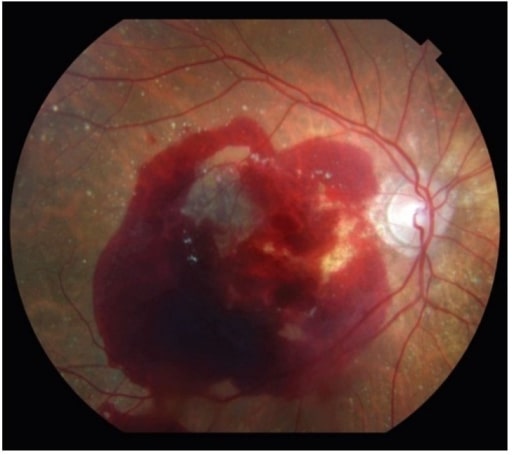
A DMI neovascular também se pode apresentar com uma hemorragia retiniana significativa.
Imagem: “Neovascular age-related macular degeneration” por Retina Service, Department of Ophthalmology, Massachusetts Eye and Ear Infirmary, Harvard Medical School, Boston, MA 02114, USA. Licença: CC BY 4.0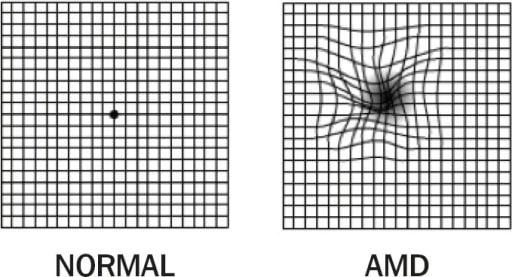
1. Teste de grelha de Amsler: visão normal (esquerda); 2. Teste de grelha de Amsler: DMI com metamorfopsias (direita). Observe as linhas distorcidas.
Imagem: “Amsler Grid” por Africa Regional Medical Advisor: Fred Hollows Foundation, Kigali, Rwanda. Licença: CC BY 2.0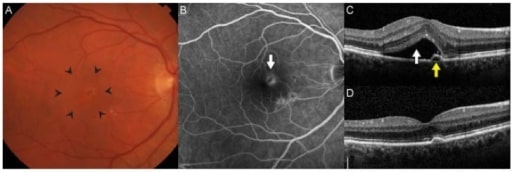
A neovascularização coroidal é característica da DMI neovascular. (A): Frequentemente há espessamento ou elevação da retina que pode ser visualizada através da biomicroscopia estereoscópica (área nas pontas das setas). (B): Na angiografia fluoresceínica, as membranas neovasculares aparecem como lesões hiperfluorescentes profundas na retina (seta) que vazam ao longo do tempo. (C): A tomografia de coerência ótica de domínio espectral permite a obtenção de imagens transversais detalhadas da anatomia da retina. Presença de líquido subretinal (seta branca) e um pequeno descolamento do epitélio pigmentar adjacente. A acuidade visual foi de 20/32. (D): Após 3 injeções intra-vítreas de Ranibizumabe com uma de frequência mensal, desaparecimento do fluido e melhoria da acuidade visual para 20/20.
Imagem: “Age-Related Macular Degeneration” por Retina Service, Department of Ophthalmology, Massachusetts Eye and Ear Infirmary, Harvard Medical School, Boston, MA 02114, USA. Licença: CC BY 4.0