O cancro do pulmão, ou seja, a transformação maligna do tecido pulmonar, é a principal causa de morte relacionada com o cancro. A maioria dos casos está associada ao tabagismo de longa duração. A doença é geralmente classificada histologicamente como cancro do pulmão de pequenas células ou cancro do pulmão de células não pequenas. O perfil molecular da neoplasia permite distinguir melhor o seu comportamento biológico, o seu prognóstico e opções de tratamento. Os sintomas incluem tosse, dispneia, perda de peso e desconforto no peito. A disseminação regional e metastática causa sintomas e complicações adicionais dependendo do local e órgão(s) afetado(s). As síndromes paraneoplásicas relacionadas incluem hipercalcemia, hiponatremia, síndrome de Lambert-Eaton, síndrome de Cushing, polimiosite e dermatomiosite. O diagnóstico definitivo e o estadiamento são feitos por biópsia, pesquisa de mutação genética com pesquisa de biomarcadores e exames de imagem. O tratamento é orientado pelo estadio e pelo perfil molecular associado. O cancro do pulmão tem um prognóstico globalmente mau.
Last updated: Dec 15, 2025
Subtipos:
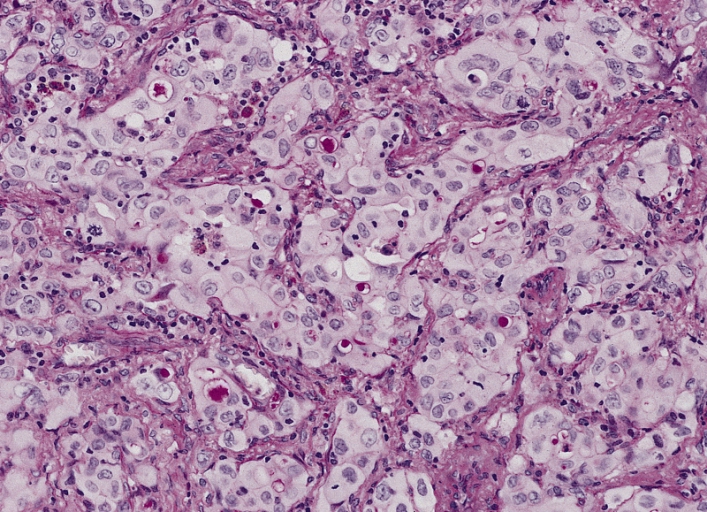
Adenocarcinoma do pulmão:
Um adenocarcinoma (sólido) pouco diferenciado, com muitas células com vacúolos de mucina
Subtipos:
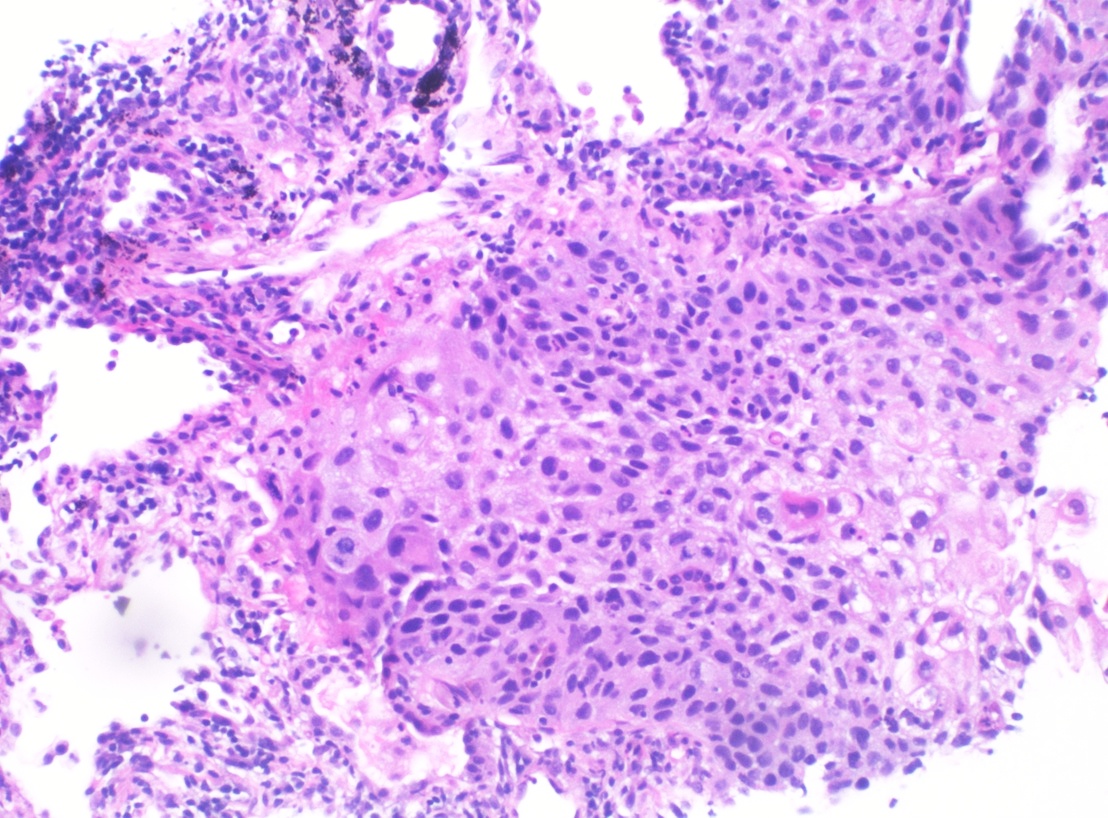
Biópsia pulmonar do carcinoma de células escamosas:
Histopatologia de carcinoma de células escamosas pouco diferenciada do pulmão (coloração de H&E)
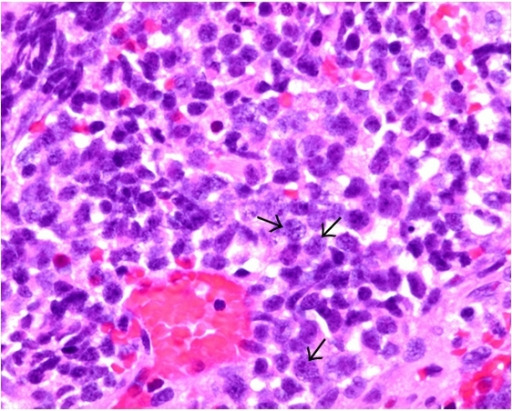
Carcinoma de pequenas células:
As células tumorais (ver setas) apresentam características de carcinoma de pequenas células, que incluem moldagem nuclear, relação aumentada de núcleo:citoplasma e núcleos finos ou com cromatina em “sal e pimenta” na coloração de H&E.
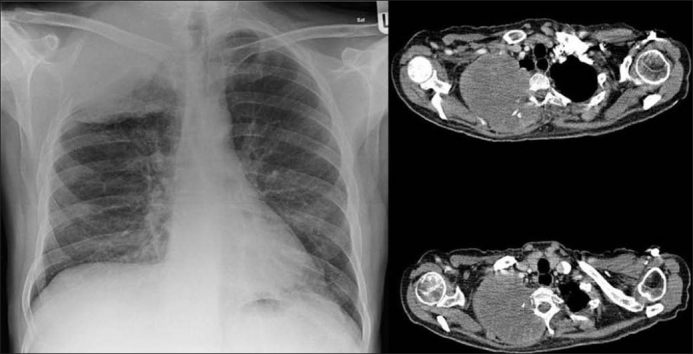
Tumor de Pancoast:
A radiografia do tórax à esquerda mostra uma neoplasia pulmonar direita com invasão da costela e da parede torácica. A tomografia computorizada à direita mostra o tumor com invasão das costelas, da parede torácica e das vértebras torácicas.
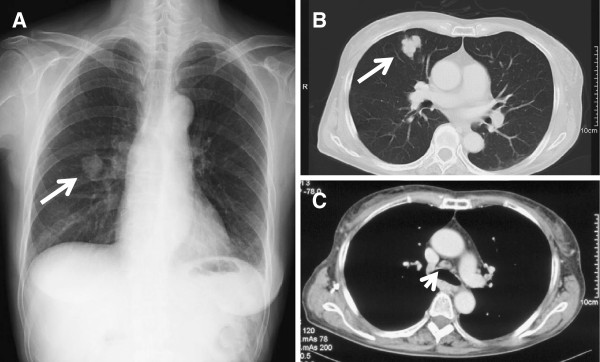
Radiografia de tórax e tomografia computorizada no momento do diagnóstico:
(A): Radiografia do tórax, com uma sombra na zona média direita (seta).
(B, C): TC convencional do tórax com uma massa solitária de 30 mm em S5 do pulmão direito (seta) e uma linfadenopatia mediastínica (ponta da seta).
Além da TC, são utilizadas as seguintes modalidades na determinação da extensão da doença para estadiamento:
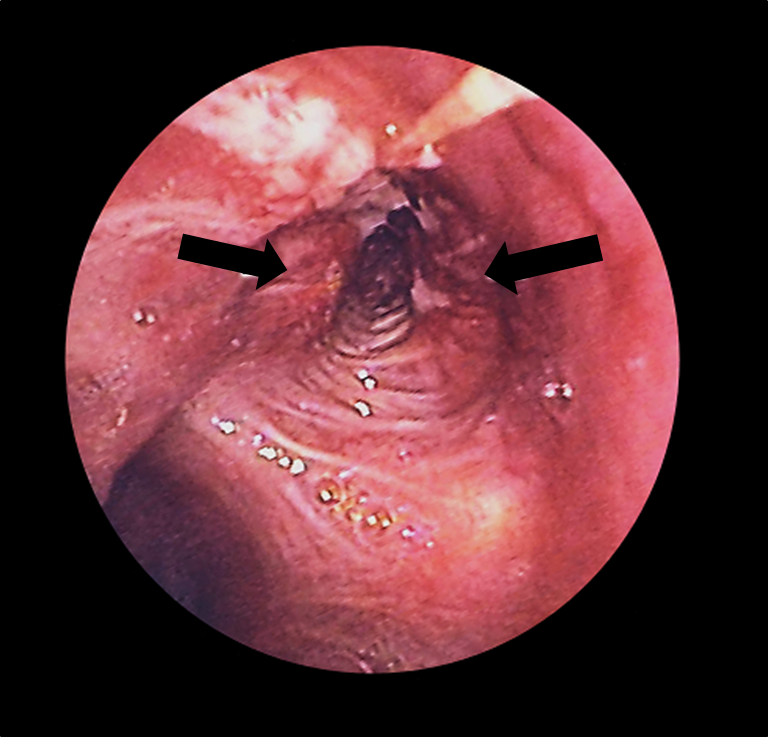
Broncoscopia:
Cancro do pulmão (setas) no brônquio esquerdo, observado num broncoscópio
Possíveis achados no cancro do pulmão:
A seguir estão as diretrizes da 8ª edição da Associação Internacional para o Estudo do Cancro do Pulmão:
| Estadio | Descrição |
|---|---|
| Tx | O tumor Tumor Inflammation primário não consegue ser avaliado. |
| T0 | Sem evidência de tumor Tumor Inflammation primário |
| Tis | Carcinoma in situ |
| T1 |
Tumor
Tumor
Inflammation ≤ 3 cm, rodeado por pulmão ou
pleura
Pleura
The pleura is a serous membrane that lines the walls of the thoracic cavity and the surface of the lungs. This structure of mesodermal origin covers both lungs, the mediastinum, the thoracic surface of the diaphragm, and the inner part of the thoracic cage. The pleura is divided into a visceral pleura and parietal pleura.
Pleura: Anatomy visceral, sem invasão do brônquio principal:
|
| T2 |
Tumor
Tumor
Inflammation > 3 cm mas ≤ 5 cm, ou:
|
| T3 T3 A T3 thyroid hormone normally synthesized and secreted by the thyroid gland in much smaller quantities than thyroxine (T4). Most T3 is derived from peripheral monodeiodination of T4 at the 5′ position of the outer ring of the iodothyronine nucleus. The hormone finally delivered and used by the tissues is mainly t3. Thyroid Hormones | Tumor Tumor Inflammation > 5 cm mas ≤ 7 cm, ou nódulos tumorais associados no mesmo lobo que o tumor Tumor Inflammation primário, ou invasão direta da parede torácica, nervo frénico ou pericárdio parietal Parietal One of a pair of irregularly shaped quadrilateral bones situated between the frontal bone and occipital bone, which together form the sides of the cranium. Skull: Anatomy |
| T4 T4 The major hormone derived from the thyroid gland. Thyroxine is synthesized via the iodination of tyrosines (monoiodotyrosine) and the coupling of iodotyrosines (diiodotyrosine) in the thyroglobulin. Thyroxine is released from thyroglobulin by proteolysis and secreted into the blood. Thyroxine is peripherally deiodinated to form triiodothyronine which exerts a broad spectrum of stimulatory effects on cell metabolism. Thyroid Hormones | Tumor Tumor Inflammation > 7 cm, ou nódulos tumorais associados num lobo ipsilateral diferente do tumor Tumor Inflammation primário, ou invasão do diafragma, mediastino, coração, grandes vasos, traqueia, esófago, nervo laríngeo recorrente, corpo vertebral ou carina |
| Estadio | Descrição |
|---|---|
| Nx | Incapaz de avaliar os gânglios linfáticos regionais |
| N0 | Sem metástases ganglionares regionais |
| N1 | Envolvimento dos gânglios linfáticos peribrônquicos e/ou hilares e dos gânglios intrapulmonares |
| N2 | Envolvimento dos gânglios linfáticos do mediastino ipsilateral e/ou subcarínicos |
| N3 | Envolvimento dos gânglios no mediastino contralateral, do hilo contralateral, do escaleno ipsilateral ou contralateral, ou dos gânglios linfáticos supraclaviculares |
| Estadio | Descrição |
|---|---|
| M0 | Sem metástases à distância |
| M1 | Metástases à distância:
|
| Agrupamento de estadios | Estadio TNM |
|---|---|
| Oculto |
|
| 0 |
|
| I |
|
| II |
|
| III |
|
| IV |
|
| Estadiamento (CPPC) | Descrição |
|---|---|
| Doença limitada |
|
| Doença extensa |
|
Cirurgia:
Quimioterapia:
Radioterapia:
Terapêuticas dirigidas:
Imunoterapia:
| Estadiamento (CPCNP) | Abordagem terapêutica |
|---|---|
| Estadio I-II |
|
| Estadio III |
|
| Estadio IV* |
|
| Estadiamento (CPPC) | Descrição |
|---|---|
| Doença limitada |
|
| Doença extensa* |
|
A modificação dos fatores de risco é mais MAIS Androgen Insensitivity Syndrome eficaz do que o rastreio na redução da morte por cancro do pulmão.