O cancro cervical, também conhecido como cancro do colo do útero ou carcinoma cervical invasivo (CCI), é o terceiro tipo de cancro ginecológico mais MAIS Androgen Insensitivity Syndrome comum em mulheres no mundo, sendo que > 50% dos casos são fatais. Nos Estados Unidos, o CCI é o 13º cancro mais MAIS Androgen Insensitivity Syndrome comum e a causa de < 3% de todas as mortes por cancro, devido à progressão lenta das lesões precursoras e, mais MAIS Androgen Insensitivity Syndrome importante, ao rastreio eficaz do cancro. Existem 2 tipos histológicos principais de CCI: carcinoma de células escamosas (ou carcinoma espinocelular - CEC) e adenocarcinoma. Causa de vírus do papiloma humano de alto risco ( hrHPVs hrHPVs Cervical Cancer, pela sigla em inglês) > 99% dos CEC e > 85% dos adenocarcinomas. A neoplasia cervical precoce é assintomática e o diagnóstico é feito através de métodos de rastreio de rotina, incluindo o teste Papanicolau cervical com citologia, teste de hrHPV e biópsia. O tratamento de lesões precursoras ou displásicas depende da gravidade da displasia e da idade do doente. O tratamento dos CCI depende do estádio e varia desde biópsia excisional por biópsia em cone cervical, para CCI microinvasivo, até histerectomia radical para casos mais MAIS Androgen Insensitivity Syndrome avançados. Se houver disseminação extracervical, recomenda-se a radioterapia e quimioterapia.
Last updated: Dec 15, 2025
Os vírus do papiloma humano de alto risco (hrHPV, “vírus oncogénicos”) estão fortemente associados a lesões de alto grau e progressão para cancro invasivo.
Relacionado com HPV HPV Human papillomavirus (HPV) is a nonenveloped, circular, double-stranded DNA virus belonging to the Papillomaviridae family. Humans are the only reservoir, and transmission occurs through close skin-to-skin or sexual contact. Human papillomaviruses infect basal epithelial cells and can affect cell-regulatory proteins to result in cell proliferation. Papillomavirus (HPV):
Não relacionado com HPV HPV Human papillomavirus (HPV) is a nonenveloped, circular, double-stranded DNA virus belonging to the Papillomaviridae family. Humans are the only reservoir, and transmission occurs through close skin-to-skin or sexual contact. Human papillomaviruses infect basal epithelial cells and can affect cell-regulatory proteins to result in cell proliferation. Papillomavirus (HPV):
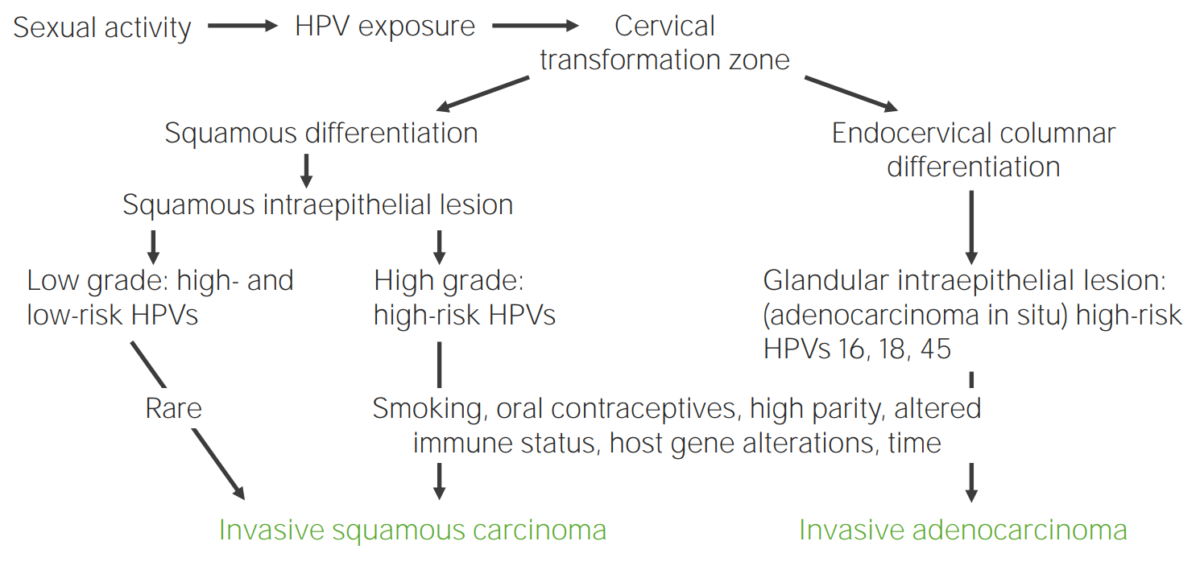
Diagrama que demonstra a patogénese do carcinoma cervical causado por HPV
Imagem por Lecturio.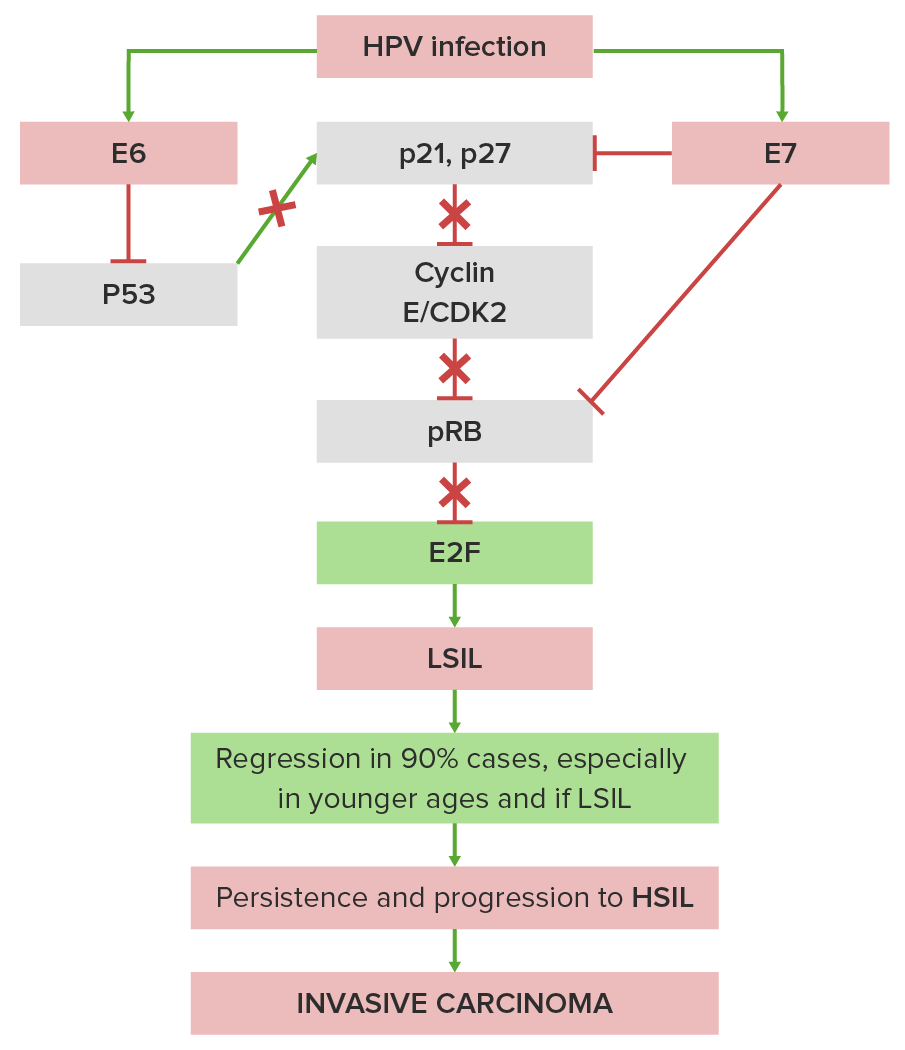
Patogénese simplificada da neoplasia intraepitelial cervical e cancro cervical:
A proteína E6 do HPV bloqueia a proteína supressora tumoral p53 (a “guardiã do genoma”), que interfere nas defesas celulares, e a proteína E7 do HPV bloqueia a proteína supressora tumoral RB, que permite o crescimento celular descontrolado. Este fenómeno perturba o equilíbrio geralmente controlado entre fatores de crescimento normais (por exemplo, pelo fator de crescimento epidérmico e fator de crescimento derivado de plaquetas) e inibidores de crescimento normal (por exemplo, por pTGF-β (fator de crescimento transformador β) e p53).
X indica onde o HPV bloqueia as vias estimulatórias ou inibitórias normais.
CDK2: quinase 2 dependente de ciclina
Classificação SIL:
Aparência macroscópica do HSIL:
Aparência microscópica:
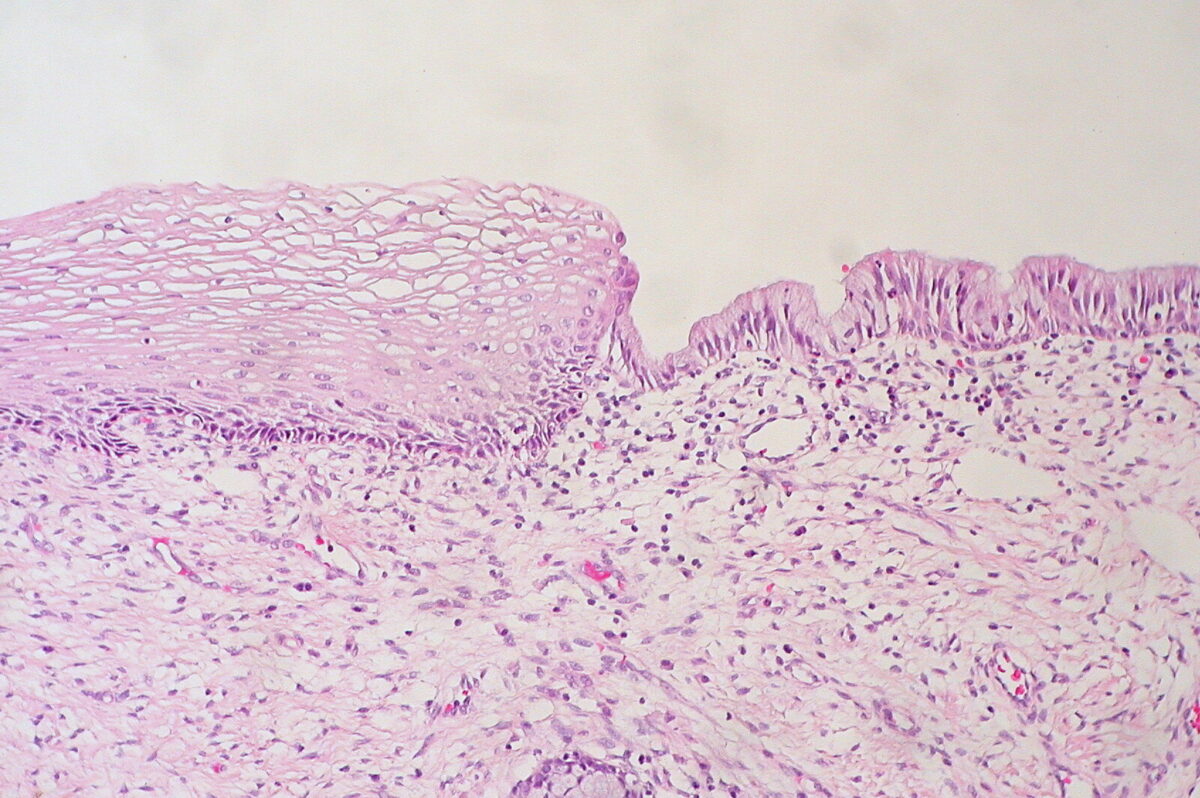
Achados histológicos de um colo do útero normal
Imagem: “Cervix Uteri: Normal Squamocolumnar Junction” por Ed Uthman. Licença: CC BY 2.0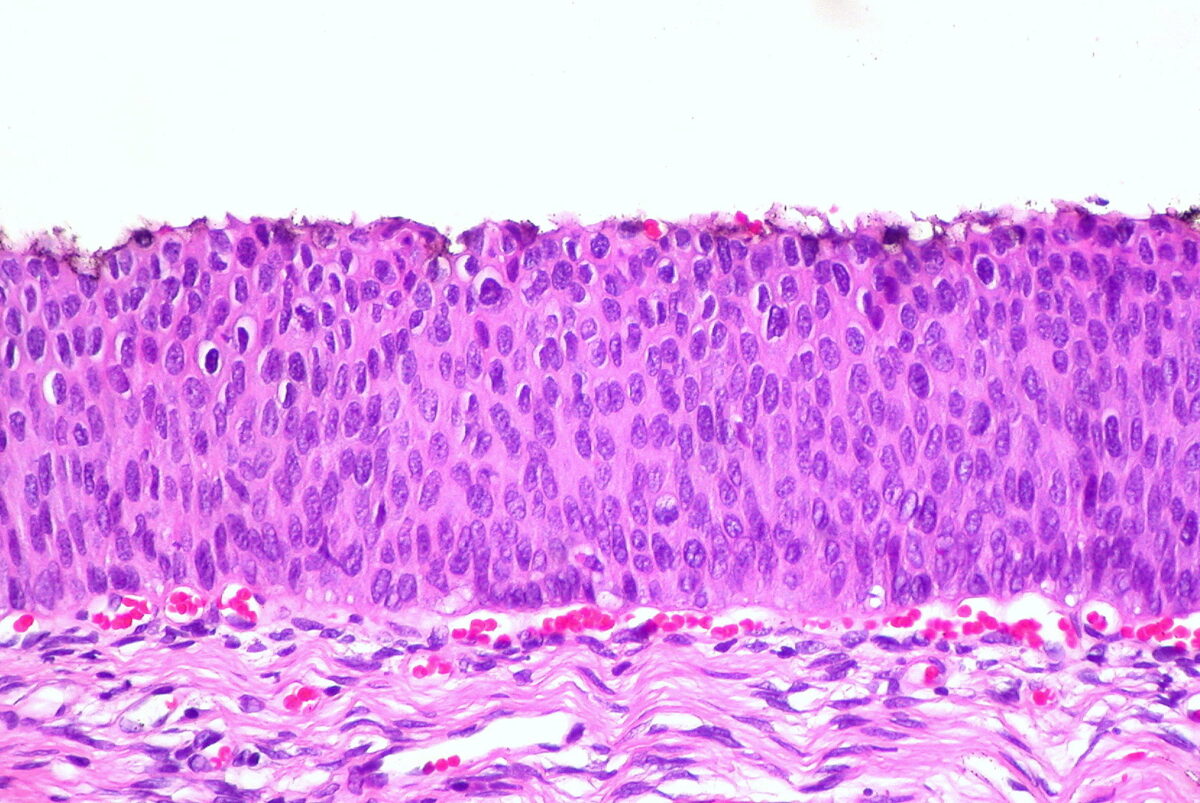
Achados histológicos em HSIL/CIN 3
Imagem: “CIN 3, Cervical Biopsy” por Ed Uthman. Licença: CC BY 2.0
Exemplos de achados de células escamosas na citologia cervical:
(a): célula normal
(b): células escamosas atípicas de significado indeterminado
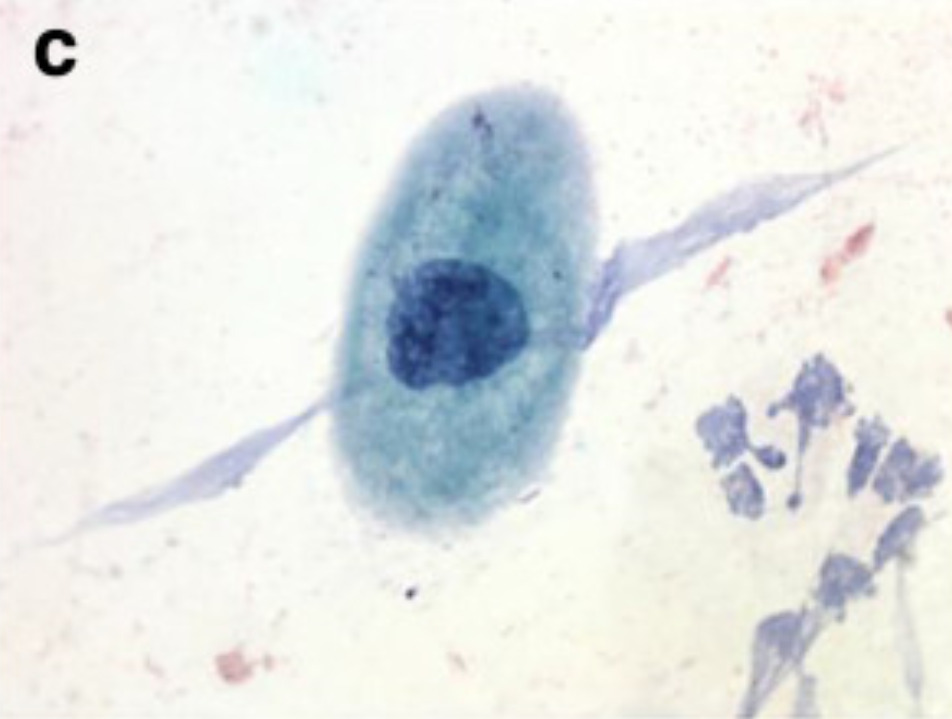
Exemplos de achados de células escamosas na citologia cervical:
(c): LSIL
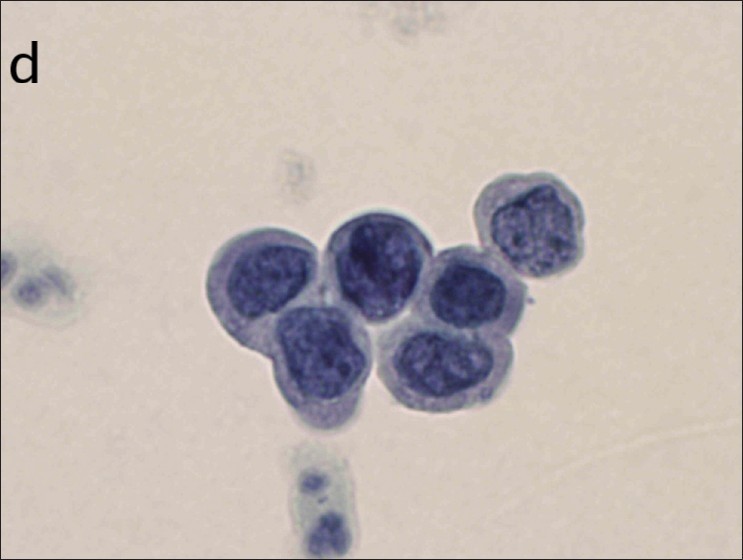
Exemplos de achados de células escamosas na citologia cervical:
(d): HSIL
Aparência macroscópica:
Aparência microscópica:
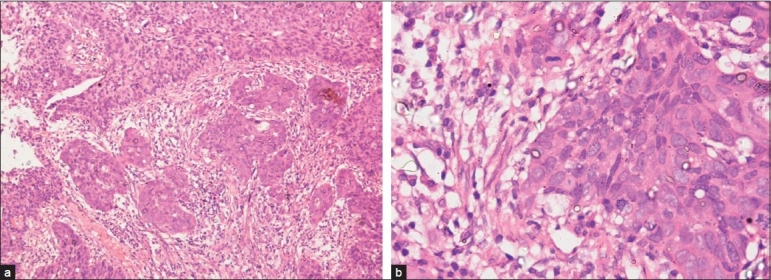
Imagens micrográficas de carcinoma cervical:
(a): exame histopatológico de uma amostra de biópsia por punção, mostra CEC não queratinizante de células grandes
(b): exame histopatológico de grande amplificação de uma biópsia por punção, mostra CEC não queratinizante de células grandes
Sinais e sintomas causados pela extensão e invasão do tumor Tumor Inflammation:
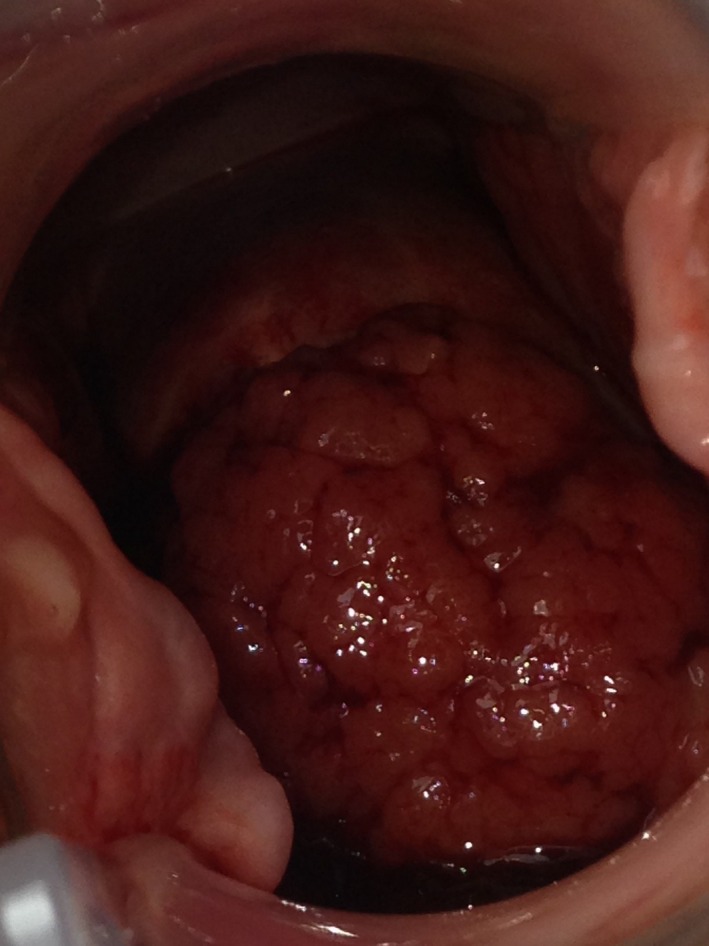
Um adenocarcinoma cervical progressivo:
A imagem mostra uma massa de progressão rápida que se projeta do colo do útero.
O diagnóstico de CCI é feito por exame histológico de uma biópsia cervical.
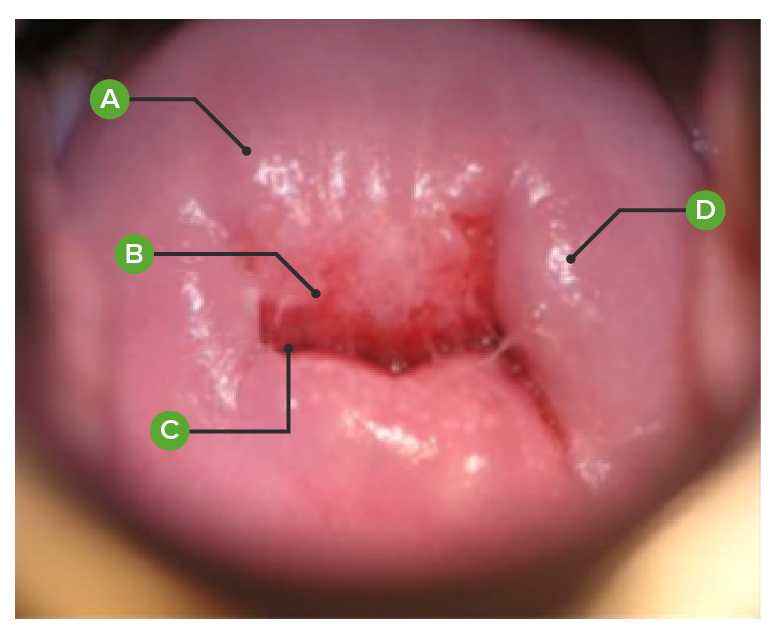
Colo do útero normal, conforme visto na colposcopia:
(A): mucosa exocervical
(B): zona de transformação entre a exocérvix e a endocérvix
(C): mucosa endocervical aparece no orifício cervical externo
(D): quisto de naboth (quisto preenchido por muco)
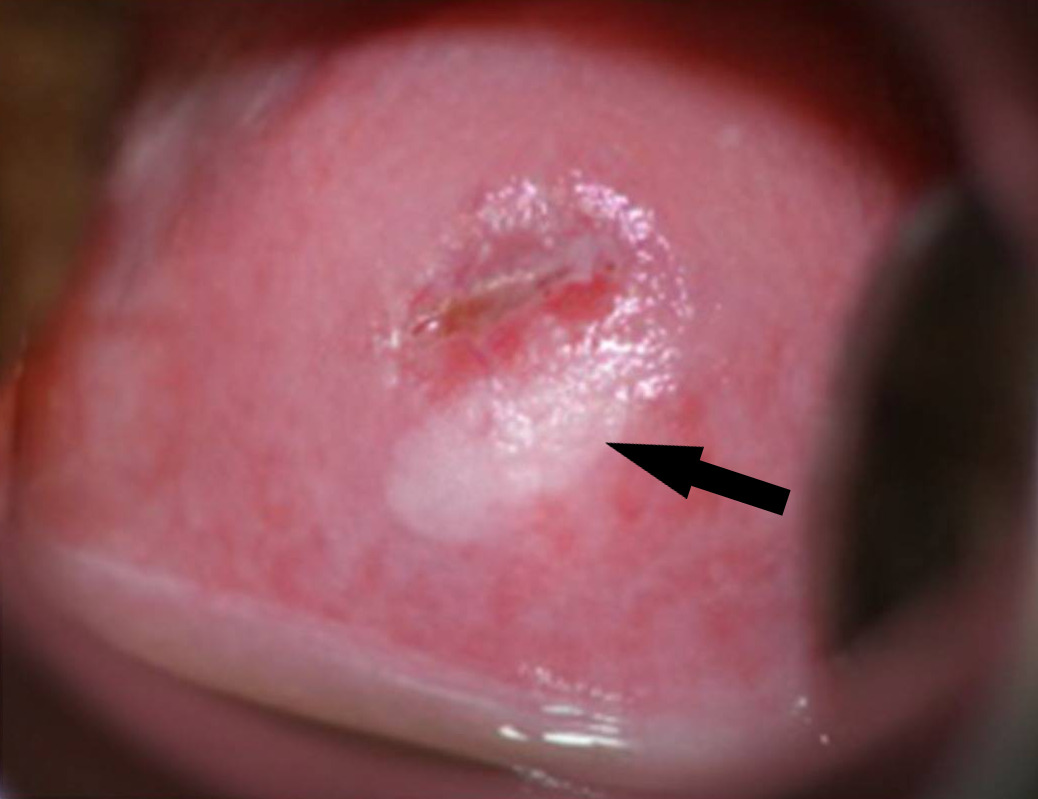
SIL do colo do útero na colposcopia:
SIL ovoide localizado na área entre as 4 e as 8 horas do colo do útero (seta). A área afetada está realçada pela aplicação de ácido acético, que deixa a área branca. Esta lesão é chamada lesão acetobranca. De notar que o bordo superior da lesão está no bordo da área glandular endocervical a cor rosa mais forte (a zona de transformação). O pequeno orifício exocervical indica que a mulher não teve parto vaginal.
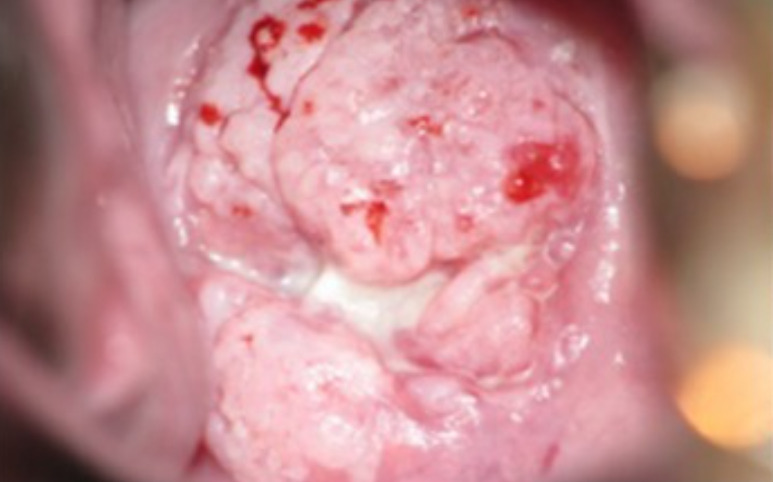
CEC invasivo do colo do útero, que está quase totalmente apagado de forma que é praticamente imperceptível: Observar a vascularização e a aparente friabilidade do tumor.
Imagem: “Population-level scale-up of cervical cancer prevention services in a low-resource setting: development, implementation, and evaluation of the cervical cancer prevention program in Zambia” por Parham GP, Mwanahamuntu MH, Kapambwe S, Muwonge R, Bateman AC, Blevins M, Chibwesha CJ, Pfaendler KS, Mudenda V, Shibemba AL, Chisele S, Mkumba G, Vwalika B, Hicks ML, Vermund SH, Chi BH, Stringer JS, Sankaranarayanan R, Sahasrabuddhe VV. Licença: CC BY 4.0, editado pela Lecturio.| Estádio do tumor Tumor Inflammation (T) | Descrição |
|---|---|
| TX | O tumor Tumor Inflammation primário não pode ser avaliado |
| T0 | Sem evidência de tumor Tumor Inflammation |
| T1 | Restrito ao útero
|
| T2 | Invasão para além do útero, mas não para a parede pélvica ou parte inferior da
vagina
Vagina
The vagina is the female genital canal, extending from the vulva externally to the cervix uteri internally. The structures have sexual, reproductive, and urinary functions and a rich blood supply, mainly arising from the internal iliac artery.
Vagina, Vulva, and Pelvic Floor: Anatomy
|
| T3 T3 A T3 thyroid hormone normally synthesized and secreted by the thyroid gland in much smaller quantities than thyroxine (T4). Most T3 is derived from peripheral monodeiodination of T4 at the 5′ position of the outer ring of the iodothyronine nucleus. The hormone finally delivered and used by the tissues is mainly t3. Thyroid Hormones | Extensão para a parede pélvica ou parte inferior da
vagina
Vagina
The vagina is the female genital canal, extending from the vulva externally to the cervix uteri internally. The structures have sexual, reproductive, and urinary functions and a rich blood supply, mainly arising from the internal iliac artery.
Vagina, Vulva, and Pelvic Floor: Anatomy ou causa hidronefrose
|
| T4 T4 The major hormone derived from the thyroid gland. Thyroxine is synthesized via the iodination of tyrosines (monoiodotyrosine) and the coupling of iodotyrosines (diiodotyrosine) in the thyroglobulin. Thyroxine is released from thyroglobulin by proteolysis and secreted into the blood. Thyroxine is peripherally deiodinated to form triiodothyronine which exerts a broad spectrum of stimulatory effects on cell metabolism. Thyroid Hormones | Invasão da bexiga ou reto ou extensão para além da pélvis |
| Estádio do gânglio (N) | Descrição |
|---|---|
| NX | Não pode ser avaliado |
| N0 | Sem metástases nos gânglios linfáticos |
| N0 (i +) | Células cancerosas isoladas em gânglios linfáticos (≤ 0,2 mm MM Multiple myeloma (MM) is a malignant condition of plasma cells (activated B lymphocytes) primarily seen in the elderly. Monoclonal proliferation of plasma cells results in cytokine-driven osteoclastic activity and excessive secretion of IgG antibodies. Multiple Myeloma) |
| N1 | Metástase dos gânglios |
| Estádio de metástase (M) | Descrição |
|---|---|
| M0 | Sem metástases à distância |
| M1 | Metástases à distância |
O estadiamento TNM pode ser usado para determinar o grupo de estadiamento prognóstico.
| Grupo de estadiamento prognóstico | Estádio de tumor Tumor Inflammation (T) | Estádio de metástase (M) | |
|---|---|---|---|
| I | I A | T1a | M0 |
| IB | T1b | M0 | |
| II | IIA | T2a | M0 |
| IIB | T2b | M0 | |
| III | IIIA | T3a | M0 |
| IIIB | T3b | M0 | |
| IV | IVA | T4 T4 The major hormone derived from the thyroid gland. Thyroxine is synthesized via the iodination of tyrosines (monoiodotyrosine) and the coupling of iodotyrosines (diiodotyrosine) in the thyroglobulin. Thyroxine is released from thyroglobulin by proteolysis and secreted into the blood. Thyroxine is peripherally deiodinated to form triiodothyronine which exerts a broad spectrum of stimulatory effects on cell metabolism. Thyroid Hormones | M0 |
| IVB | Qualquer estádio | M1 | |
O tratamento depende do estádio, extensão para os gânglios linfáticos e tecidos próximos, e da idade da doente, estádio de gravidez e desejo de manter a fertilidade.