A agamaglobulinemia ligada ao cromossoma X, também conhecida como agamaglobulinemia de Bruton ou doença de Bruton, é um distúrbio genético recessivo raro caracterizado pelo desenvolvimento inadequado de células B, levando ao défice de células B maduras, capazes de responder à estimulação de respostas imunes mediadas por células ou por certas células apresentadoras de antigénios. A agamaglobulinemia ligada ao X é mais provável de ser encontrada em homens do que em mulheres e é causada por mutações no gene da tirosina cinase de Bruton no cromossoma X. O resultado desta mutação é uma ausência completa ou quase completa de todos os anticorpos. A apresentação inclui infeções bacterianas recorrentes após os primeiros meses de vida. O tratamento consiste em imunoglobulinas IV e uso profilático de antibióticos.
Última atualização: Feb 19, 2025
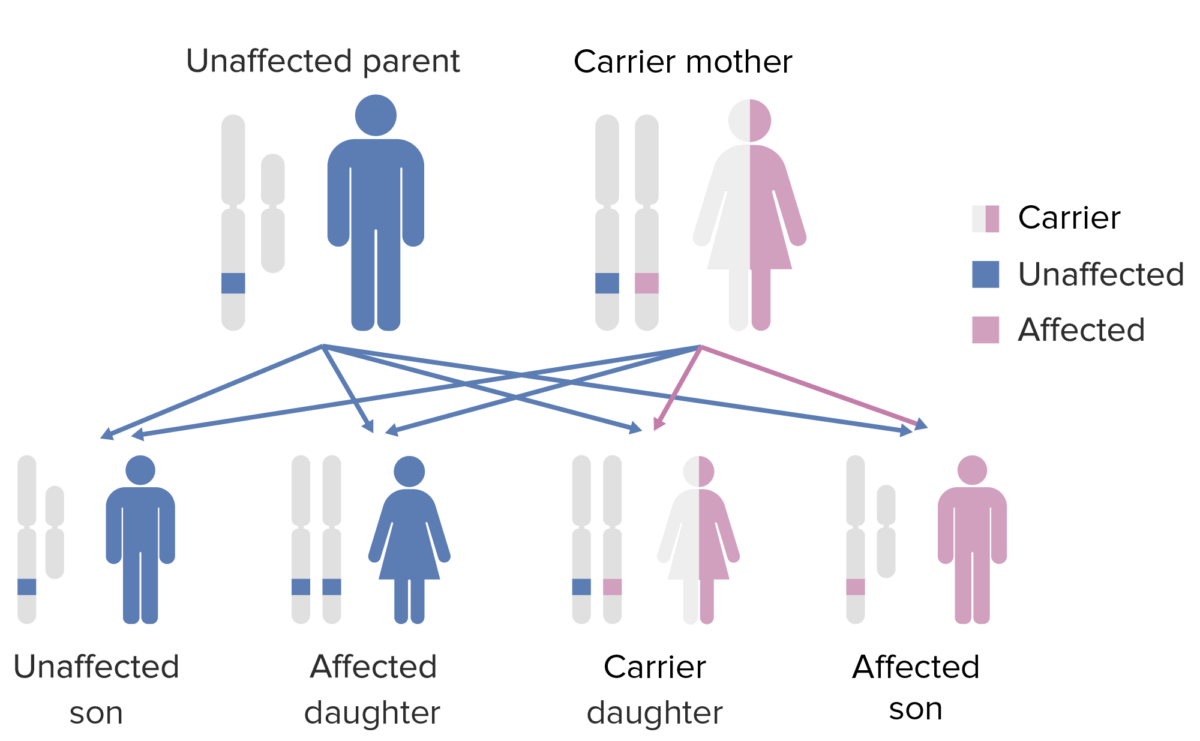
O padrão de hereditariedade da agamaglobulinemia ligada ao X:
Observar que a mãe deve contribuir com o gene X como defeito para o filho do sexo masculino para que este expresse esse fenótipo.
As seguintes condições são diagnósticos diferenciais da agamaglobulinemia ligada ao X.