El cáncer de mama es el cáncer más común en las mujeres y la 2da causa principal de muerte relacionada con el cáncer en las mujeres en Estados Unidos. La detección temprana y la mejora de los tratamientos específicos de la patología han dado lugar a una disminución de las tasas de mortalidad. Varias organizaciones brindan recomendaciones con respecto al tamizaje para grupos de riesgo y de edad específicos. El tamizaje incluye examen de las mamas, mamografía, resonancia magnética (RM) y ultrasonido.
Última actualización: Jul 16, 2022
El cáncer de mama es una enfermedad caracterizada por la transformación maligna de las células epiteliales de la mama.
Factores no modificables que aumentan el riesgo:
Factores de riesgo modificables:
Mnemotecnia:
“BReast-CAncer 1 y 2” = Los genes mutados son los genes BRCA1 y BRCA2 (cáncer de mama 1 y 2, por sus siglas en inglés).
Se necesitan detalles de los antecedentes médicos y personales del paciente para determinar su riesgo:
El riesgo de un paciente de desarrollar cáncer de mama se puede clasificar como:
Los modelos de predicción se utilizan para la categorización específica del riesgo, con consideración de más factores.
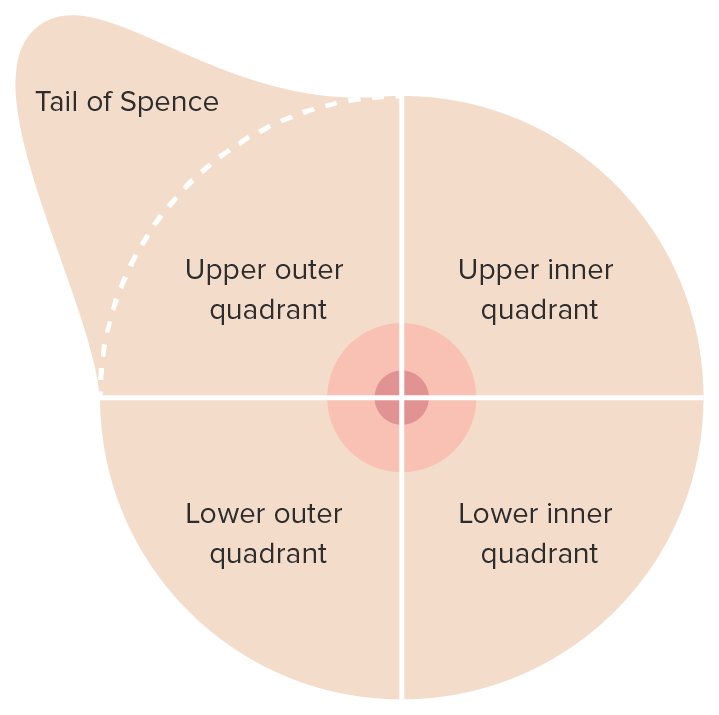
Examen clínico de la mama: localización de las lesiones mamarias por cuadrante
Imagen por Lecturio.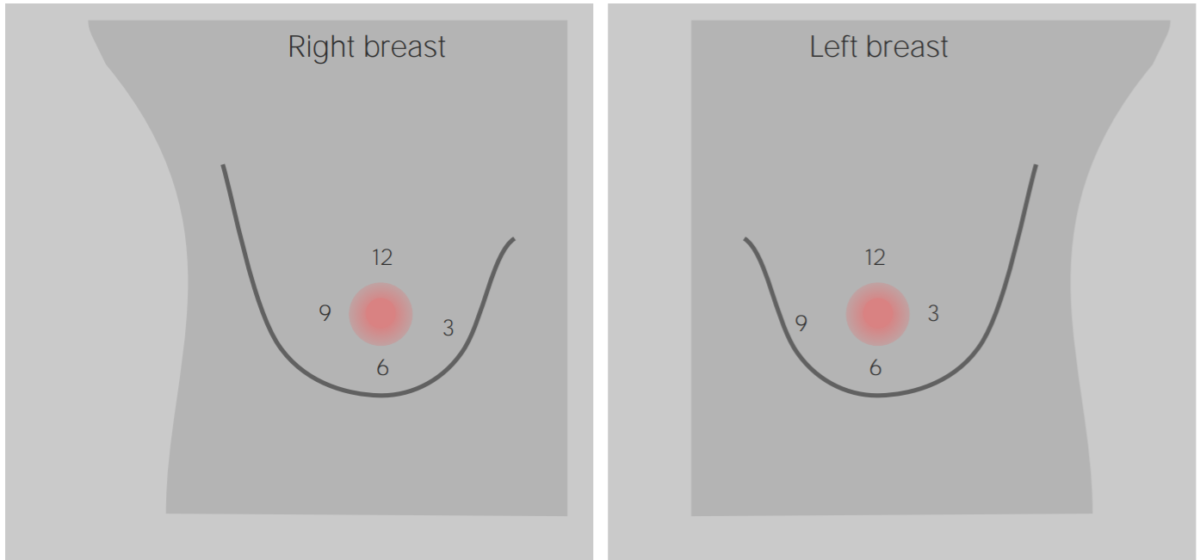
Examen clínico de las mamas: localización de las lesiones mamarias según las agujas del reloj
Imagen por Lecturio.La mamografía es el método más eficaz para detectar el cáncer de mama temprano, y demuestra de manera constante una disminución del 20%–40% en la mortalidad entre las mujeres tamizadas:
| Categoría | Evaluación | Seguimiento |
|---|---|---|
| BI-RADS 0 | Evaluación incompleta | Se necesitan vistas adicionales de la mamografía o ultrasonido de seguimiento |
| BI-RADS 1 | Negativa | Continúe con las pruebas de tamizaje de rutina. |
| BI-RADS 2 | Hallazgos benignos | Continúe con las pruebas de tamizaje de rutina. |
| BI-RADS 3 | Hallazgos probablemente benignos | Mamografía o ultrasonido diagnóstico en 6 meses |
| BI-RADS 4 | Anormalidad sospechosa | Se debe considerar realizar una biopsia. |
| BI-RADS 5 | Muy sugestiva de malignidad | Debe realizarse una biopsia. |
| BI-RADS 6 | Neoplasia maligna comprobada por biopsia | Tratamiento del cáncer de mama |
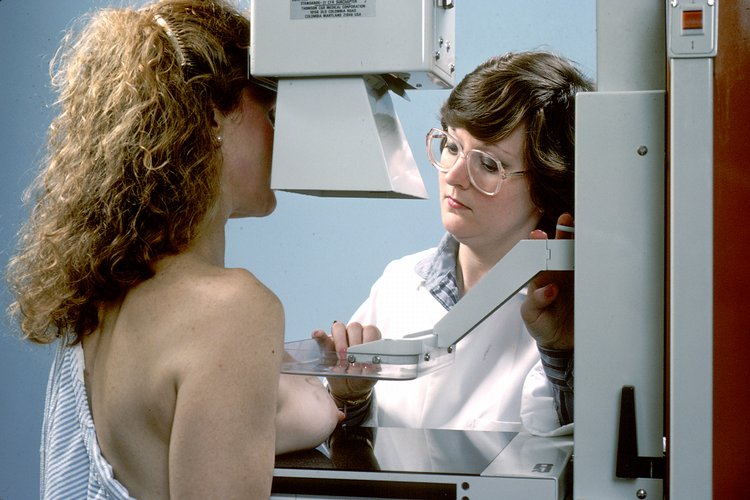
Tamizaje del cáncer de mama: una mujer que se somete a una mamografía de tamizaje
Imagen: “Mammogram” por National Cancer Institute. Licencia: Public Domain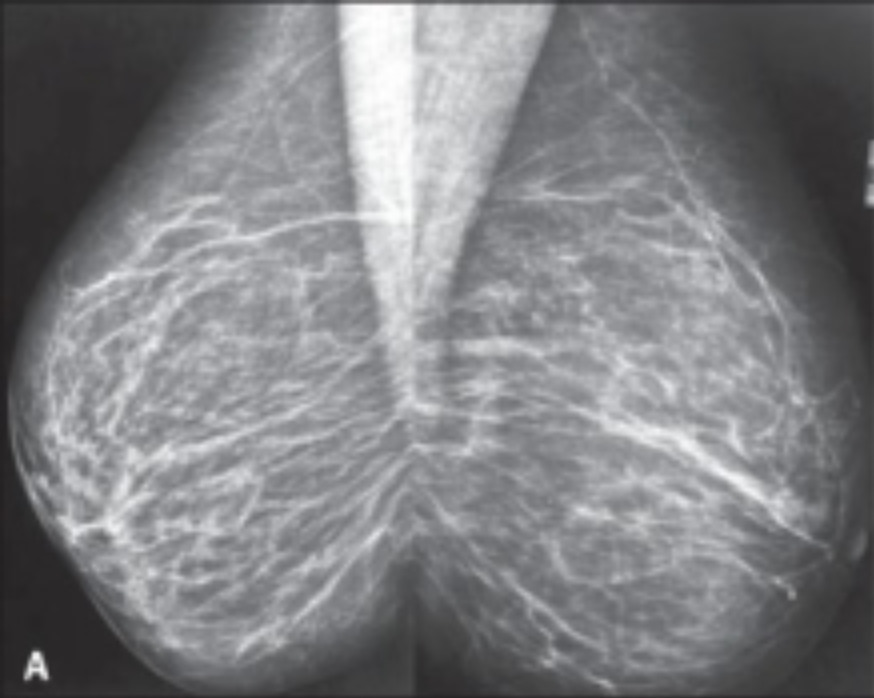
Hallazgos benignos en una mamografía Mamografía de tamizaje, proyecciones oblicuas mediolaterales derecha e izquierda, que muestran calcificaciones vasculares puntiformes, bilaterales y escasas (asociadas a vasos sanguíneos/benignas) (BI-RADS 2)
Imagen: “Fat necrosis associated with the use of oral anticoagulant therapy:atypical mammographic findings” por Radiologia Brasileira. Licencia: CC BY 4.0, edited by Lecturio.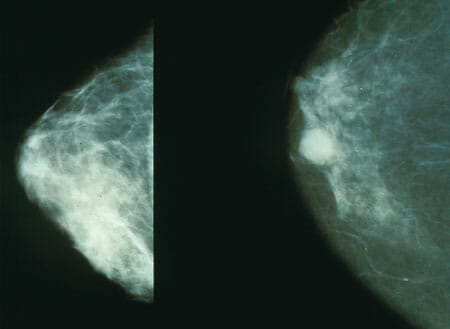
La mamografía se realiza para el tamizaje y la detección precoz del cáncer de mama:
Izquierda: imagen de mamografía de tejido mamario normal
Derecha: imagen de mamografía de tejido mamario canceroso
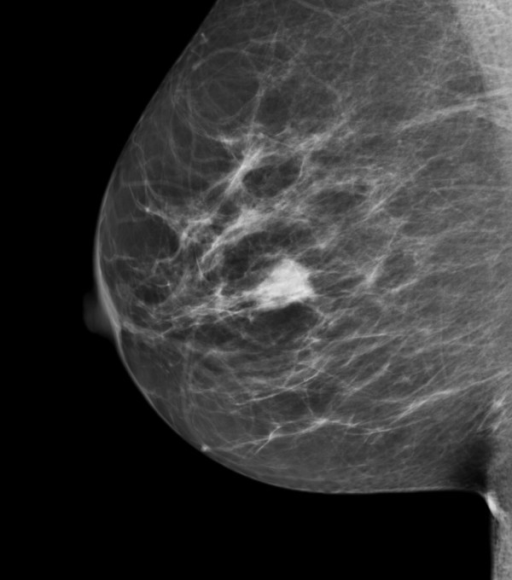
Una masa en una mamografía de tamizaje
La imagen muestra una masa circunscrita en la posición de las 3 en punto de la mama derecha.
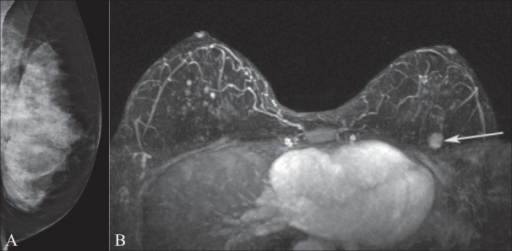
Mamografía y RM de mama
La imagen A muestra una mamografía de la mama izquierda en un portador de la mutación del gen BRCA1. Obsérvese el tejido mamario extremadamente denso.
La imagen B muestra una RM con una masa realzada (flecha) en la parte superior izquierda de la mama que estaba oculta en la mamografía.
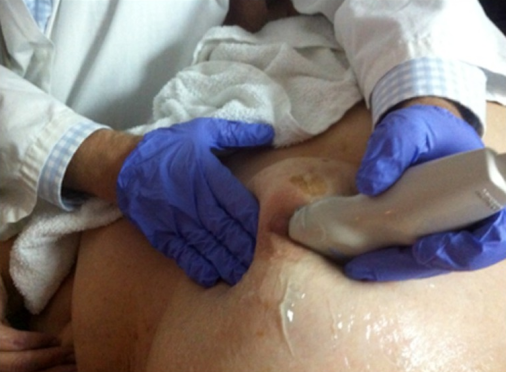
Evaluación de la mama: uso del ultrasonido
Imagen: “Retroareolar Carcinomas in Breast Ultrasound: Pearls and Pitfalls” por Cancers. Licencia: CC BY 4.0, editada por Lecturio.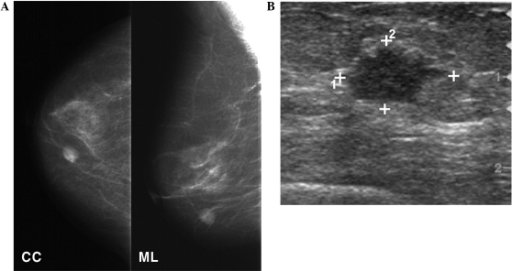
Mamografía y ultrasonido mamario
A: La mamografía muestra una masa redonda de alta densidad en el cuadrante inferior interno de la mama derecha.
B: El seguimiento por ultrasonido muestra una masa hipoecoica de 1,3 cm de forma irregular en la mama.
Las guías auspiciadas por las sociedades y por el gobierno difieren en:
| Organización | Mamografía | Examen clínico de mama |
|---|---|---|
| USPSTF |
|
Evidencia insuficiente |
| ACP |
|
No recomendado |
| ACS |
|
No recomendado |
| ACOG |
|
|
| NCCN |
|
|
Recomendaciones:
Asesoramiento y pruebas genéticas (USPSTF) :
No quirúrgico
Quirúrgico: mastectomía profiláctica
Se debe asesorar a las mujeres sobre la posible morbilidad de los procedimientos quirúrgicos (menopausia quirúrgica, libido, imagen corporal).
Los portadores masculinos de BRCA tienen un mayor riesgo de cáncer de mama, próstata y páncreas: