El síndrome de Zellweger, también llamado síndrome cerebrohepatorrenal, es un raro trastorno congénito de la biosíntesis de los peroxisomas y se considera un error innato del metabolismo. El síndrome de Zellweger es la forma más grave de un espectro de afecciones denominado trastorno del espectro de Zellweger, y se caracteriza por la reducción o ausencia de peroxisomas funcionales. Los síntomas están presentes desde el momento del nacimiento e incluyen hipotonía, mala alimentación, convulsiones y ciertos rasgos físicos distintivos, especialmente características faciales y malformaciones esqueléticas. No hay cura para el síndrome de Zellweger. La tasa media de supervivencia es inferior a un año.
Última actualización: Dic 17, 2024
Las manifestaciones clínicas del síndrome de Zellweger están presentes al nacer.
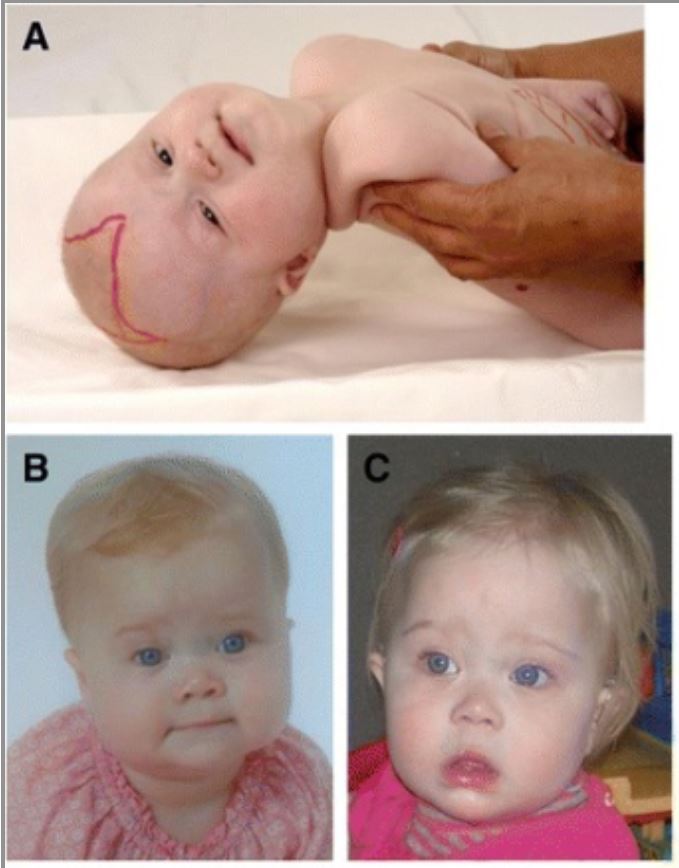
Rasgos dismórficos craneofaciales en pacientes con trastorno del espectro de Zellweger (ZSD)
Una niña de 6 meses (A) con dismorfia craneofacial típica, pliegues epicánticos, frente alta, puente nasal ancho, rebordes supraorbitales hipoplásicos y fontanela anterior grande (dibujada). Imágenes (B) y (C) muestran a una niña con ZSD a la edad de 9 meses (B) y 14 meses (C). El dismorfismo facial en esta niña es menos pronunciado.
No hay cura ni tratamiento eficaz para el síndrome de Zellweger. El tratamiento es de soporte en el mejor de los casos.
La muerte suele producirse en el plazo de 1 año tras el nacimiento (normalmente < 6 meses), normalmente debido a una insuficiencia respiratoria.
El síndrome de Zellweger forma parte de un grupo clínico de trastornos de la biogénesis del peroxisoma conocido como trastorno del espectro de Zellweger. Todas las siguientes enfermedades también tienen una herencia autosómica recesiva, y se diagnostican y tratan de forma similar al síndrome de Zellweger:
El diagnóstico diferencial del síndrome de Zellweger es muy amplio. Las características clínicas, pruebas bioquímicas, imagenología y, en última instancia, las pruebas genéticas ayudan a diferenciar y proporcionar un diagnóstico. Los siguientes son trastornos que deben considerarse en cualquier neonato que presente una hipotonía profunda: