El síndrome de Peutz-Jeghers (SPJ) es un trastorno hereditario autosómico dominante que se caracteriza por la presencia de pólipos gastrointestinales y máculas mucocutáneas pigmentadas. El síndrome de Peutz-Jeghers es uno de los síndromes de poliposis, un grupo de afecciones heredadas o adquiridas que se caracterizan por el crecimiento de pólipos en el tracto gastrointestinal y que se asocian a otras características extracolónicas. Los síndromes están causados por mutaciones en genes específicos asociados a la supresión de tumores o a la regulación del ciclo celular. El síndrome de Peutz-Jeghers es causado por alteraciones en el gen STK11 y se asocia a cánceres colónicos (colorrectales) y no colónicos (pancreáticos, gástricos, de mama, uterinos, cervicales, de pulmón, de ovarios y de testículos). El manejo es con vigilancia estrecha y cirugía.
Última actualización: Ene 11, 2024
El síndrome de Peutz-Jeghers (SPJ) es un trastorno hereditario autosómico dominante caracterizado por pólipos hamartomatosos gastrointestinales y máculas melanóticas en piel y mucosas.
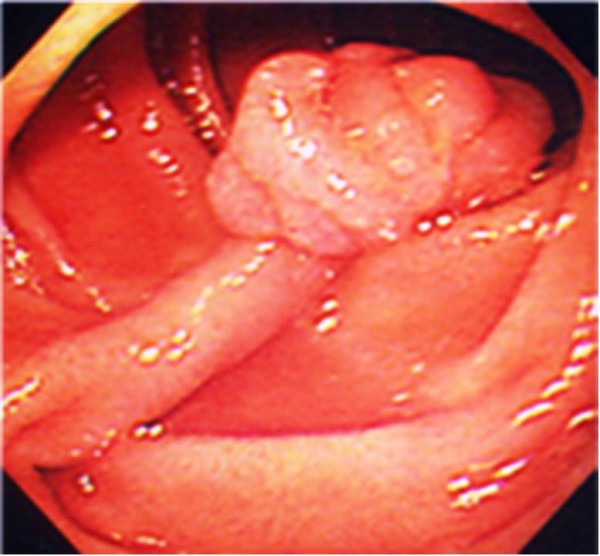
Pólipo hamartomatoso solitario típico del síndrome de Peutz-Jeghers
Imagen: “Pedunculated duodenal polyp measuring 15 mm in diameter in the second part of the duodenum” por Yusuke Sekino, et al. Licencia: CC BY 2.0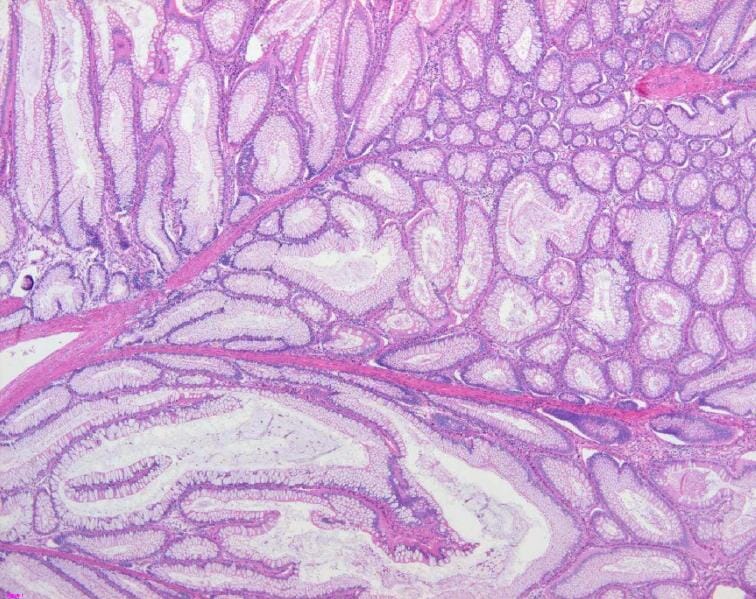
Hallazgos patológicos de un pólipo de Peutz-Jeghers: El pólipo colónico muestra un epitelio mucoso hiperplásico y un patrón arborizante de músculo liso, consistente con un pólipo hamartomatoso (tinción H&E, 200x).
Imagen: “Colon histology with Peutz-Jeghers polyp” por Jong-Ha Yoo et al. Licencia: CC BY 2.0