El raquitismo hipofosfatémico ligado al cromosoma X (XLHR, por sus siglas en inglés) es el más común de varios trastornos hereditarios y se caracteriza por la pérdida renal de fosfato, que da lugar a huesos débiles o blandos. Anteriormente conocida como "raquitismo resistente a la vitamina D", el XLHR no se considera actualmente una verdadera resistencia a la vitamina D (relacionada con defectos hereditarios en la vía metabólica de la vitamina D o en el receptor del calcitriol). Las presentaciones clínicas típicas ocurren durante la infancia y se manifiestan como baja estatura, genu valgo o genu varo, dolor óseo y dolor dental. El diagnóstico se realiza mediante estudios de laboratorio y se confirma con la identificación de la mutación en el gen PHEX. El tratamiento incluye burosumab o dosis altas de vitamina D activada (calcitriol) y fosfato. El monitoreo del paciente por parte de un equipo multidisciplinario es crucial para garantizar el crecimiento adecuado.
Última actualización: Jul 17, 2022
El raquitismo hipofosfatémico ligado al cromosoma X (XLHR, por sus siglas en inglés) es un trastorno genético raro que causa hipofosfatemia y raquitismo clínico resultante.
La presentación clínica del XLHR puede variar de asintomática a gravemente sintomática. El raquitismo hipofosfatémico ligado al cromosoma X suele confundirse con el raquitismo nutricional en los bebés, y los síntomas incluyen:
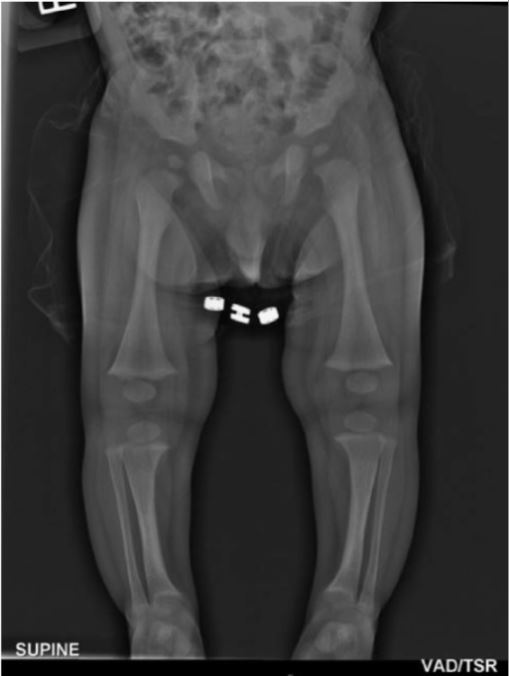
Un lactante de 7 meses con raquitismo hipofosfatémico ligado al cromosoma X:
Los huesos largos de las extremidades inferiores muestran un ensanchamiento de las metáfisis con aspecto deteriorado, pero sin ampliación de la epífisis. También hay un leve arqueo de la tibia.
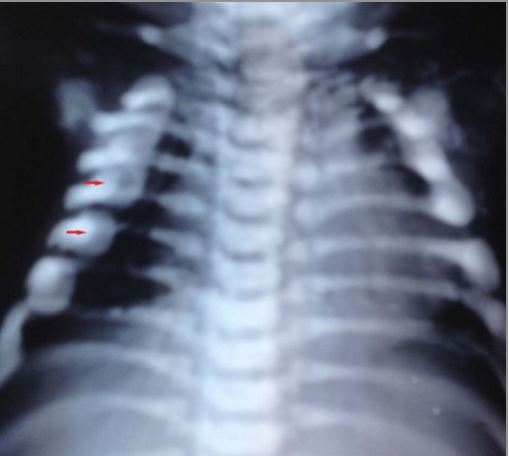
Radiografía que muestra el rosario raquítico
Imagen: «Malignant infantile osteopetrosis: Case report with review of literature» por Essabar L, Meskini T, Ettair S, Erreimi N, Mouane N. Licencia: CC BY 2.0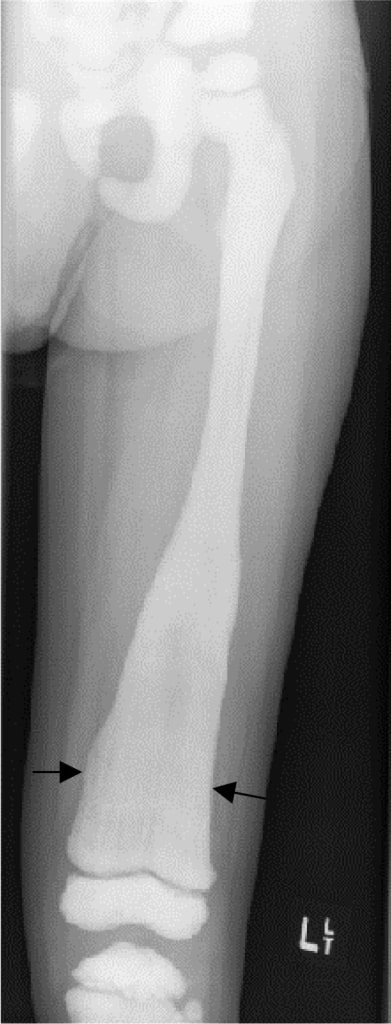
Un niño de 4 años con deformidad en matraz de Erlenmeyer del fémur distal
Imagen: «Osteopetrosis» por Stark Z, Savarirayan R. Licencia: CC BY 2.0Antecedentes familiares:
Pruebas de laboratorio:
Pruebas genéticas:
Imagenología:
Debe realizarse una evaluación radiológica para descartar arqueo fisiológico y displasia ósea. Los posibles hallazgos radiográficos pueden ser:
Los objetivos del tratamiento son mejorar la osteomalacia y las deformidades del esqueleto, mejorar el crecimiento de los bebés y la actividad física de los niños, así como disminuir el dolor.
Algunos adultos con XLHR podrían tener problemas médicos mínimos, mientras que otros pueden experimentar molestias persistentes o complicaciones. Es imprescindible monitorear el tratamiento para detectar posibles complicaciones del hiperparatiroidismo y la nefrocalcinosis.