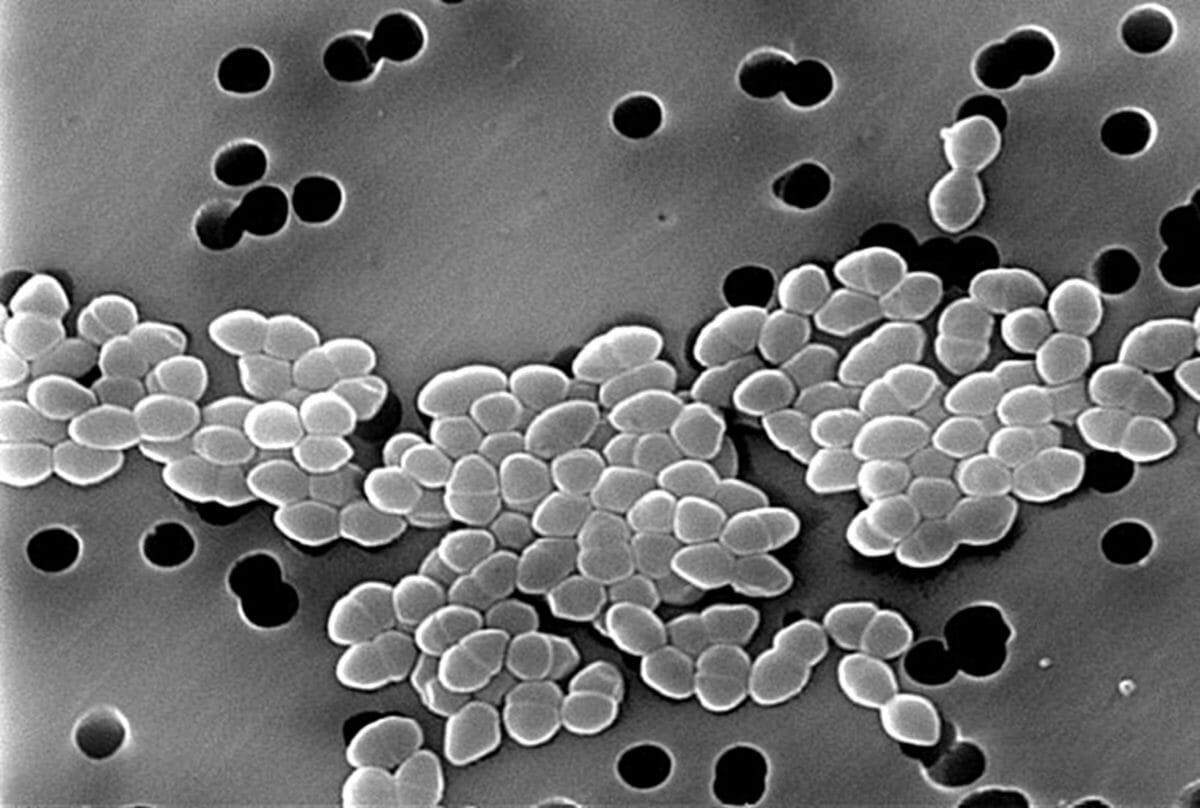
Los organismos multirresistentes y las infecciones nosocomiales son un problema sanitario mundial y una causa importante de morbilidad y mortalidad. Los organismos multirresistentes son microorganismos, principalmente bacterias, que son resistentes/no susceptibles a ≥1 agente en ≥3 categorías de clase antimicrobiana. Se incluyen en este grupo el Staphylococcus aureus resistente a la meticilina, los enterococos resistentes a la vancomicina, las bacterias Gram negativas productoras de betalactamasas de espectro extendido (BLEE, por sus siglas en inglés), las Pseudomonas aeruginosa difíciles de tratar/resistentes y las Enterobacterias resistentes a los carbapenémicos (e.g. Escherichia coli, Salmonella y Klebsiella). Dado que la terapia antibiótica para los organismos multidrogorresistentes es limitada, se recomiendan medidas preventivas como la administración de antibióticos y el control de la infección. Las infecciones nosocomiales, también denominadas infecciones "asociadas a la atención en salud" o "adquiridas en el hospital", son infecciones transmitidas en EN Erythema nodosum is an immune-mediated panniculitis (inflammation of the subcutaneous fat) caused by a type IV (delayed-type) hypersensitivity reaction. It commonly manifests in young women as tender, erythematous nodules on the shins. Erythema Nodosum un hospital o centro sanitario y que no existían en EN Erythema nodosum is an immune-mediated panniculitis (inflammation of the subcutaneous fat) caused by a type IV (delayed-type) hypersensitivity reaction. It commonly manifests in young women as tender, erythematous nodules on the shins. Erythema Nodosum el momento del ingreso. Entre ellas se encuentran las infecciones relacionadas con catéteres intravasculares, las infecciones del tracto urinario asociadas a catéteres, la neumonía adquirida en EN Erythema nodosum is an immune-mediated panniculitis (inflammation of the subcutaneous fat) caused by a type IV (delayed-type) hypersensitivity reaction. It commonly manifests in young women as tender, erythematous nodules on the shins. Erythema Nodosum el hospital, la neumonía asociada a la ventilación, las infecciones por Clostridioides difficile y las infecciones del sitio quirúrgico. Los LOS Neisseria factores de riesgo para desarrollar estas infecciones son la hospitalización, la residencia en EN Erythema nodosum is an immune-mediated panniculitis (inflammation of the subcutaneous fat) caused by a type IV (delayed-type) hypersensitivity reaction. It commonly manifests in young women as tender, erythematous nodules on the shins. Erythema Nodosum un centro sanitario de larga duración, el uso frecuente de antibióticos y las comorbilidades subyacentes.
Last updated: Jul 17, 2023
Contents
Excluyendo la transmisión nosocomial del SARS-CoV-2 durante la pandemia, las nfecciones asociadas a la atención en EN Erythema nodosum is an immune-mediated panniculitis (inflammation of the subcutaneous fat) caused by a type IV (delayed-type) hypersensitivity reaction. It commonly manifests in young women as tender, erythematous nodules on the shins. Erythema Nodosum salud no bacterianas son menos frecuentes que las bacterianas.
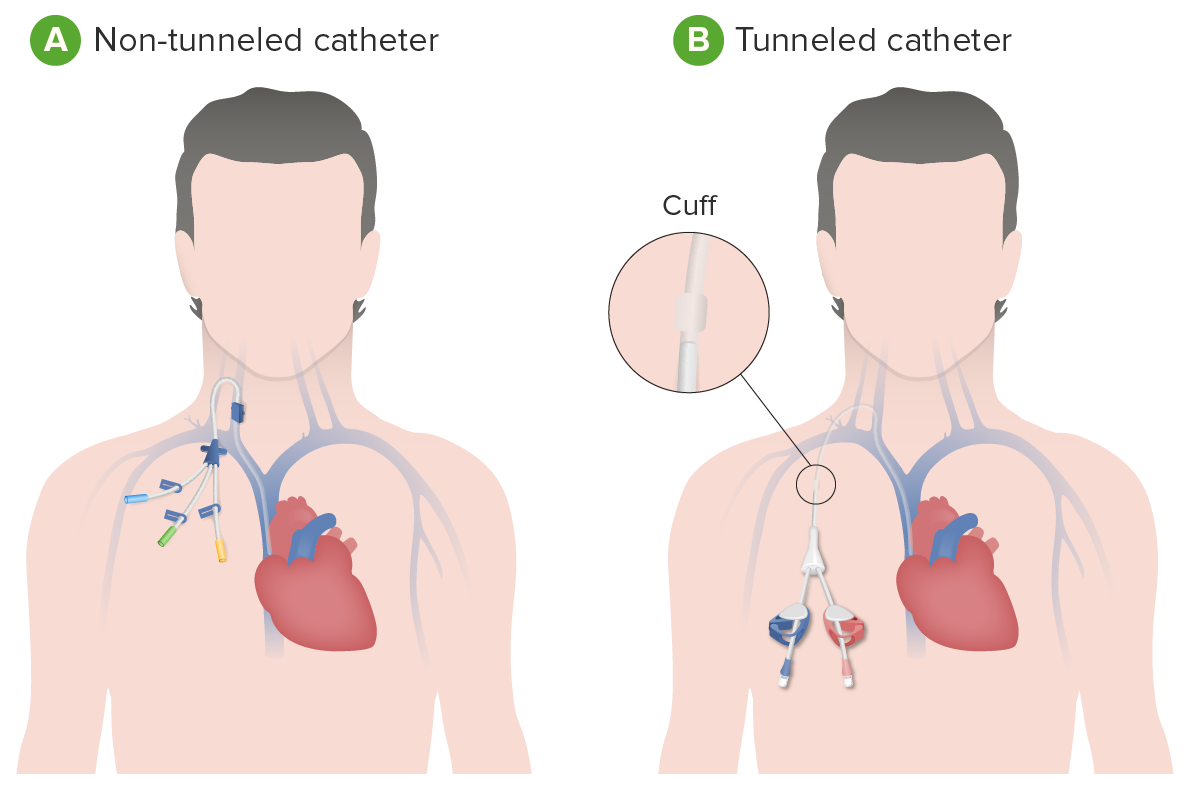
Un catéter venoso central (e.g., catéter de diálisis) es una fuente potencial de infección:
A: catéter no tunelizado (diseñado para ser temporal y puede colocarse en una vena grande cerca del cuello, tórax o la ingle)
B: Catéter de diálisis tunelizado (colocado debajo de la piel) (pensado para ser utilizado durante más tiempo)
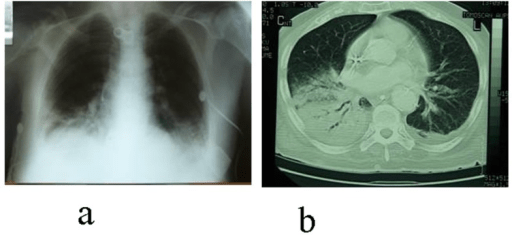
Neumonía asociada al ventilador:
a: Radiografía de tórax que muestra neumonía en la base del pulmón derecho
b: La TC del tórax revela un absceso pulmonar en desarrollo con pleuritis y aparente empiema en la zona observada en la radiografía de tórax.
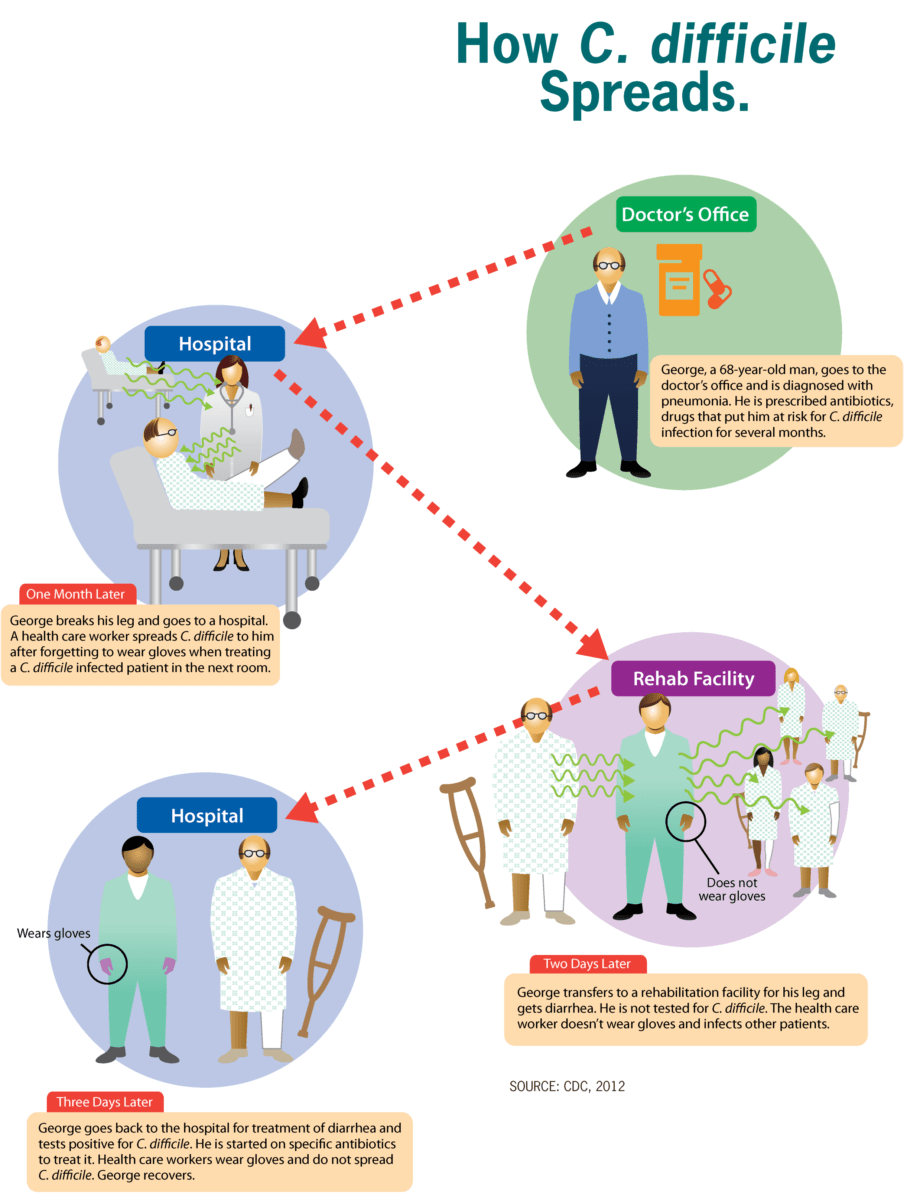
La imagen muestra cómo Clostridioides difficile (C. difficile) se propaga por el medio ambiente, favoreciendo entornos sanitarios como hospitales y centros de rehabilitación.
Imagen: “How C. difficile spreads” por CDC. Licencia: Dominio Público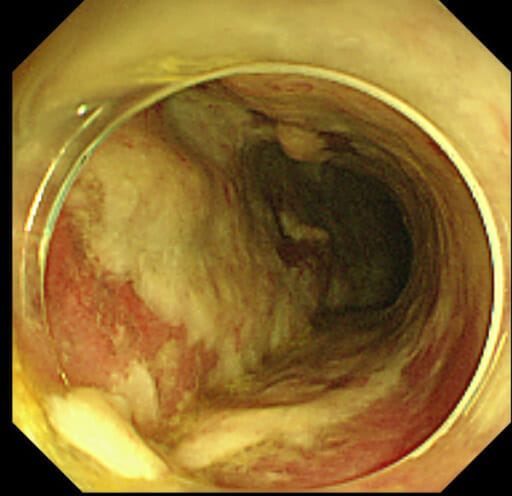
Colitis pseudomembranosa debida a una infección por C. difficile: la colonoscopia demuestra una pared colónica cubierta por pseudomembranas gruesas, que consisten en placas irregulares de material fibrinopurulento y epitelio mucoso desprendido que recubren la mucosa intestinal roja e inflamada.
Imagen: “Colonoscopy on the fifth postoperative day” por Department of Surgery, Jichi Medical University Saitama Medical Center. Licencia: CC BY 2.0