La hemocromatosis hereditaria es un trastorno autosómico recesivo asociado con mayor frecuencia a mutaciones del gen HFE. Los pacientes tienen aumentada la absorción intestinal de hierro y el depósito de hierro en varios órganos, como el hígado, el corazón, la piel y el páncreas. La presentación clínica incluye la tríada de cirrosis, diabetes y bronceado de la piel. Otros hallazgos dependen del órgano u órganos involucrados. El diagnóstico consiste en estudios de hierro, que muestran elevación de transferrina y ferritina. Se recomienda el tamizaje genético entre los miembros de la familia. Se realiza imagenología y estudios invasivos dependiendo de las complicaciones asociadas. El tratamiento requiere flebotomía (o terapia de quelación de hierro en algunos casos) para prevenir la progresión de la enfermedad. El pronóstico es bueno para los pacientes que se encuentran en las etapas tempranas de la enfermedad y que están bajo tratamiento. La presencia de fibrosis hepática es un factor de mal pronóstico.
Última actualización: Ene 17, 2024
La hemocromatosis hereditaria es:
Es importante tener en cuenta que las causas de la sobrecarga de hierro pueden superponerse u ocurrir al mismo tiempo.
Trastornos de sobrecarga de hierro secundarios (adquiridos):
Ciertas condiciones requieren una disminución o aumento en la absorción de hierro y el hierro circulante, una vía regulada por la hepcidina:
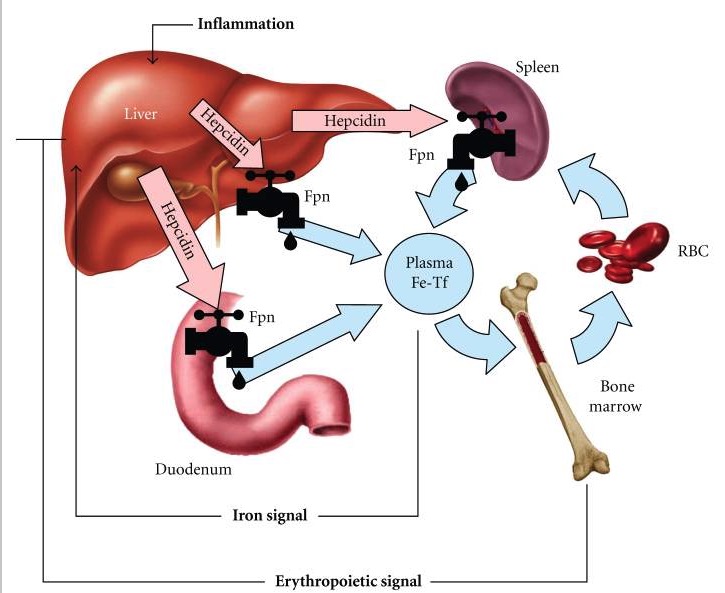
La interacción hepcidina-ferroportina determina el flujo de hierro al plasma.
1. El hierro de la dieta se capta intestinalmente en el duodeno.
2. El hierro se mueve desde el duodeno a través del transportador de hierro, ferroportina, y entra a la circulación a través de transferrina.
3. La transferrina lleva al hierro a la médula ósea para la síntesis de hemoglobina.
4. A medida que los eritrocitos envejecen, son fagocitados por macrófagos (principalmente en el bazo), liberando hierro nuevamente a la circulación a través de ferroportina.
5. Cuando hay un aumento de hierro o inflamación, aumenta la hepcidina, lo que reduce la absorción duodenal de hierro y la liberaciónb de hierro por la degradación de eritrocitos viejos.
6. Cuando se necesita una mayor formación de eritrocitos, la eritropoyetina inhibe la hepcidina para permitir una mayor absorción de hierro (desde el intestino) y liberar hierro desde los macrófagos con eritrocitos envejecidos.
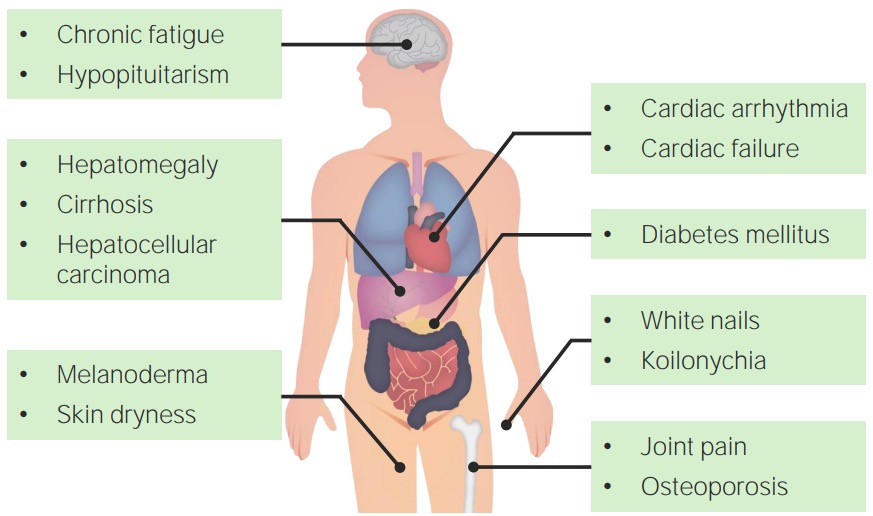
Características clínicas de la hemocromatosis.
Imagen por Lecturio.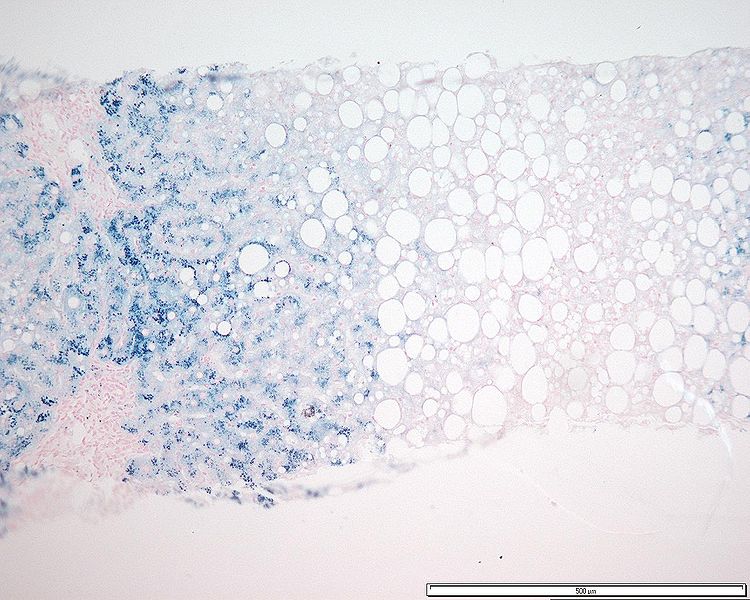
Acumulación de hierro en hepatocitos en un paciente con hemocromatosis (teñido con azul de Prusia de Perls)
Imagen: “Grade 3 hepatocyte iron accumulation” por Mathew, J. et al. Licencia: CC BY 3.0.