La deficiencia de aromatasa es una afección genética muy rara con herencia autosómica recesiva. La deficiencia de aromatasa se caracteriza por una privación congénita de estrógenos con un aumento de los niveles de testosterona debido a la disminución de los niveles de la enzima aromatasa. Las mujeres afectadas presentan un desarrollo anormal de los genitales externos, virilización, amenorrea primaria y estatura elevada. Los varones suelen desarrollar síntomas más tarde en la vida, incluyendo hiperinsulinemia y trastornos del metabolismo de los lípidos. Los individuos afectados por la deficiencia de aromatasa tienen un mayor riesgo de desarrollar osteoporosis. El tratamiento consiste en una terapia de sustitución hormonal.
Última actualización: Dic 29, 2024
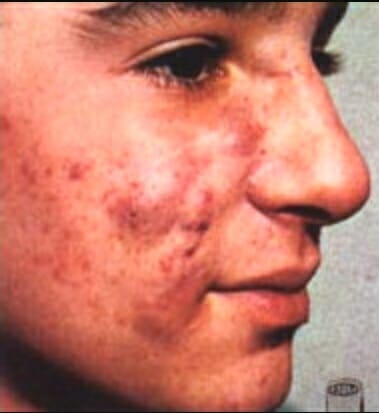
Acné por virilización durante la semana 12–30 de embarazo
Imagen: “Retoqueacne”por Jesus Angel Rey. Licencia: Dominio Público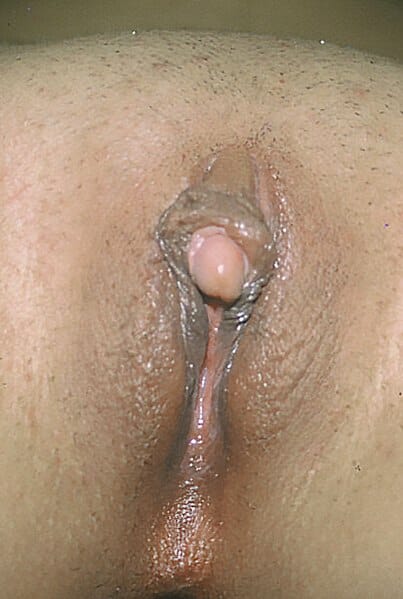
Clitoromegalia, otro signo que se produce debido a la virilización
Imagen: “Clitoromegaly” por Copcu, E, Aktas, A, Sivrioglu, N, Copcu, O, Oztan, Y. Licencia: CC BY 2.0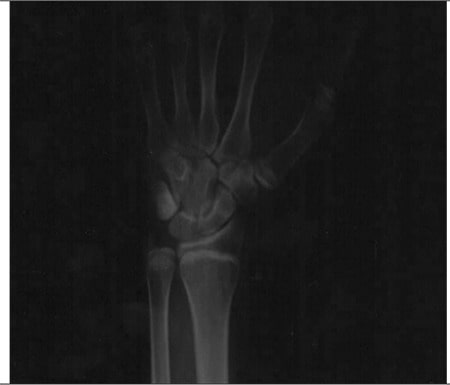
Radiografía de un hombre de 27 años con deficiencia de aromatasa
La radiografía simple de hueso de la muñeca y la mano izquierdas demuestra que las epífisis metacarpianas y de las falanges están abiertas. La edad ósea estimada es de 15 años.