Los antiestrógenos son medicamentos que disminuyen los efectos estrogénicos en el cuerpo. Los antiestrógenos incluyen los moduladores selectivos de los receptores de estrógeno (SERM, por sus siglas en inglés), los reguladores descendentes selectivos de los receptores de estrógeno (SERD, por sus siglas en inglés), los inhibidores de la aromatasa y muchos otros, que incluyen medicamentos que suprimen las gonadotropinas o contrarrestan los efectos del estrógeno. Los antiestrógenos se utilizan con mayor frecuencia en el tratamiento del cáncer de mama, pero también para tratar la pubertad precoz, la ginecomastia, la infertilidad anovulatoria y otras molestias ginecológicas. Los efectos secundarios incluyen sofocos, eventos tromboembólicos venosos, pérdida de la densidad mineral ósea y eventos cardiovasculares isquémicos. Los antiestrógenos están contraindicados en personas con reacciones de hipersensibilidad conocidas y embarazo.
Última actualización: Jun 1, 2022
Se deben considerar varias clases principales de antiestrógenos. Los medicamentos prototípicos de cada clase se indican con un asterisco (*).
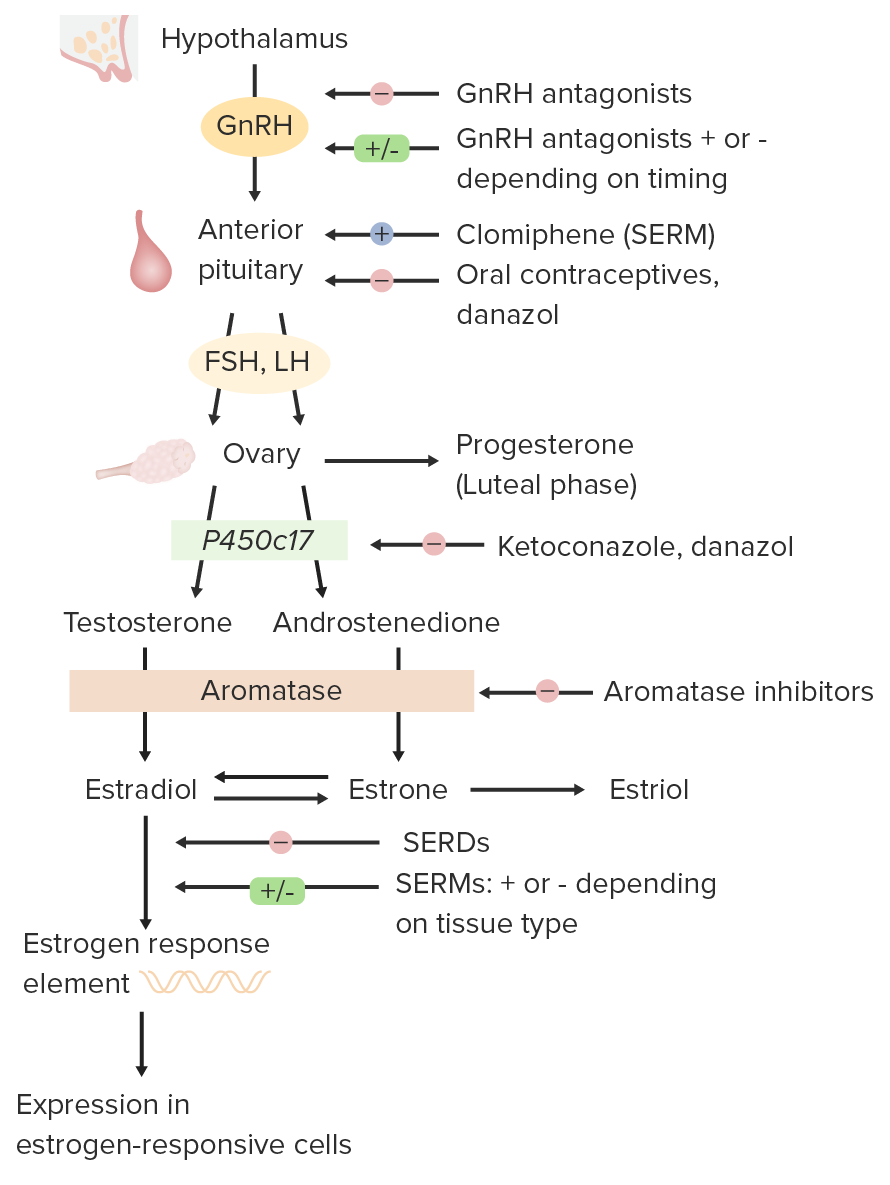
Resumen de los antiestrógenos y sus acciones asociadas
GnRH: hormona liberadora de gonadotropina
SERM: moduladores selectivos de los receptores de estrógenos
FSH: hormona foliculoestimulante
LH: hormona luteinizante
SERD: reguladores descendentes selectivos de los receptores de estrógeno
Tamoxifeno, raloxifeno, ospemifeno, bazedoxifeno y citrato de clomifeno:
Fulvestrant:
Los SERM actúan como agonistas estrogénicos en algunos tejidos y como antagonistas estrogénicos en otros.
| Tejido | Efectos normales del estrógeno | Efectos de los SERM |
|---|---|---|
| Mamas |
|
Efectos antagonistas:
|
| Hipotálamo e hipófisis | Inhibe la liberación de GnRH y de gonadotropinas (i.e., FSH, LH). | Efectos antagonistas: ↓ inhibición de FSH/LH → ↑ liberación de FSH/LH → ↑ desarrollo folicular y ovulación |
| Óseo | ↑ Densidad mineral ósea (BMD, por sus siglas en inglés) | Efectos agonistas: Protegen contra la pérdida de BMD en el estado hipoestrogénico de la menopausia. |
| Útero |
|
|
| Hígado |
|
Efectos agonistas:
|
Efectos fisiológicos de los SERD:
El fulvestrant tiene efectos puramente antiestrogénicos en los tejidos. Los efectos fisiológicos clave incluyen:
Las indicaciones principales de cada medicamento se indican con un asterisco (*):
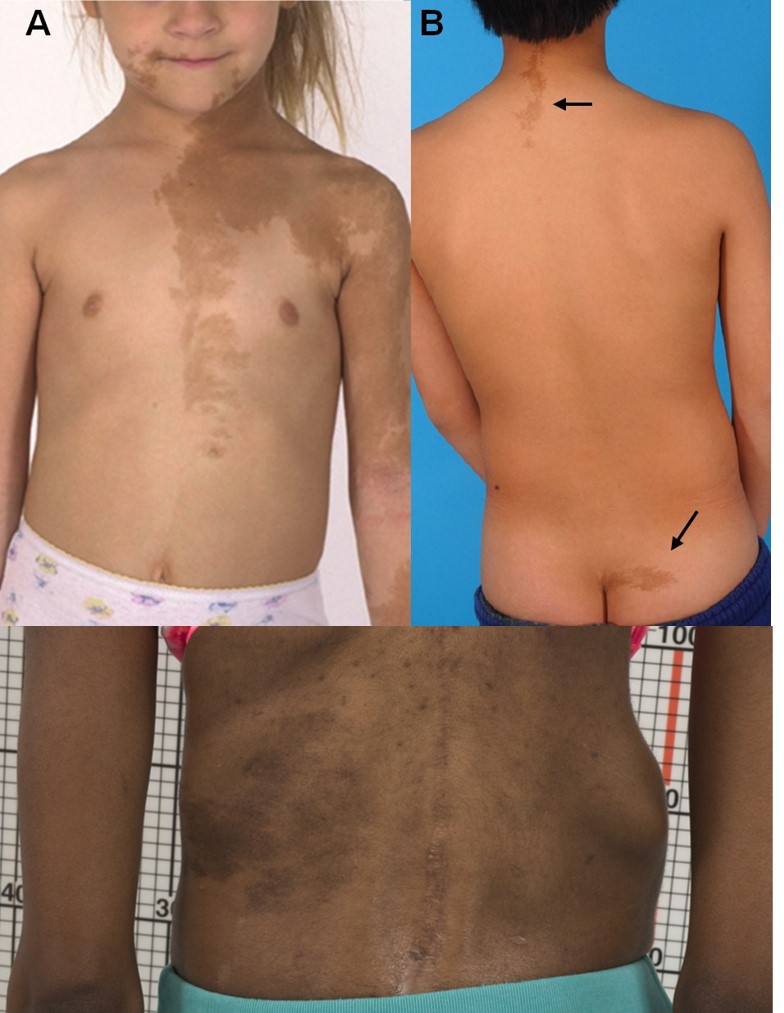
Síndrome de McCune-Albright:
El síndrome de McCune-Albright se presenta con una tríada clásica. La tríada incluye pubertad precoz periférica, displasia fibrosa ósea e hiperpigmentación café con leche de la piel, que a menudo se encuentra en la nuca y en el pliegue de las nalgas.
Los inhibidores de la aromatasa evitan la conversión de testosterona en estrógeno, el cual es un proceso conocido como aromatización. Los medicamentos de esta clase incluyen anastrozol, letrozol y exemestano. Los medicamentos se utilizan más comúnmente en el tratamiento del cáncer de mama posmenopáusico.
Anastrozol, letrozol:
Exemestano:
Leuprolida:
Ganirelix, elagolix:
| Medicamento | Clase del medicamento | Mecanismo de acción | Indicaciones | Notas |
|---|---|---|---|---|
| Moduladores selectivos de los receptores de estrógeno (SERM) | Tamoxifeno |
|
Tratamiento del cáncer de mama con receptores hormonales positivos en mujeres premenopáusicas | Aumenta el riesgo de cáncer endometrial. |
| Raloxifeno |
|
Ningún efecto significativo sobre el crecimiento endometrial | ||
| Reguladores descendentes selectivos de los receptores de estrógeno (SERD) | Fulvestrant | Antagonista competitivo «puro» de estrógenos en los receptores de estrógeno | Cáncer de mama |
|
| Inhibidores de la aromatasa | Anastrozol | Inhibidor competitivo no esteroideo de la aromatasa | Cáncer de mama en mujeres posmenopáusicas | Los efectos secundarios incluyen:
|
| Exemestano | Inhibidor irreversible de la aromatasa | |||
| Análogos de la hormona liberadora de gonadotropina (GnRH) | Leuprolida | Agonista de la GnRH → la administración continua suprime la hormona foliculoestimulante (FSH) y la hormona luteinizante (LH). |
|
|
| Elagolix | Antagonista directo de la GnRH → suprime FSH/LH. |
|
Las dosis son más bajas → los efectos secundarios de la menopausia son menores que con la leuprolida. |