La agammaglobulinemia ligada al cromosoma X, también conocida como agammaglobulinemia de Bruton o enfermedad de Bruton, es un trastorno genético recesivo poco común que se caracteriza por el desarrollo inadecuado de las células B, lo que lleva a una falta de células B maduras capaces de responder a la estimulación por respuestas inmunitarias mediadas por células o ciertas células presentadoras de antígenos. Es más probable encontrar agammaglobulinemia ligada al cromosoma X en hombres que en mujeres y se debe a mutaciones en el gen de la tirosina quinasa de Bruton en el cromosoma X. El resultado de esta mutación es una falta total o casi completa de todos los anticuerpos. La presentación incluye infecciones bacterianas recurrentes después de los primeros meses de vida. El tratamiento consiste en inmunoglobulinas intravenosas y uso profiláctico de antibióticos.
Última actualización: Feb 19, 2025
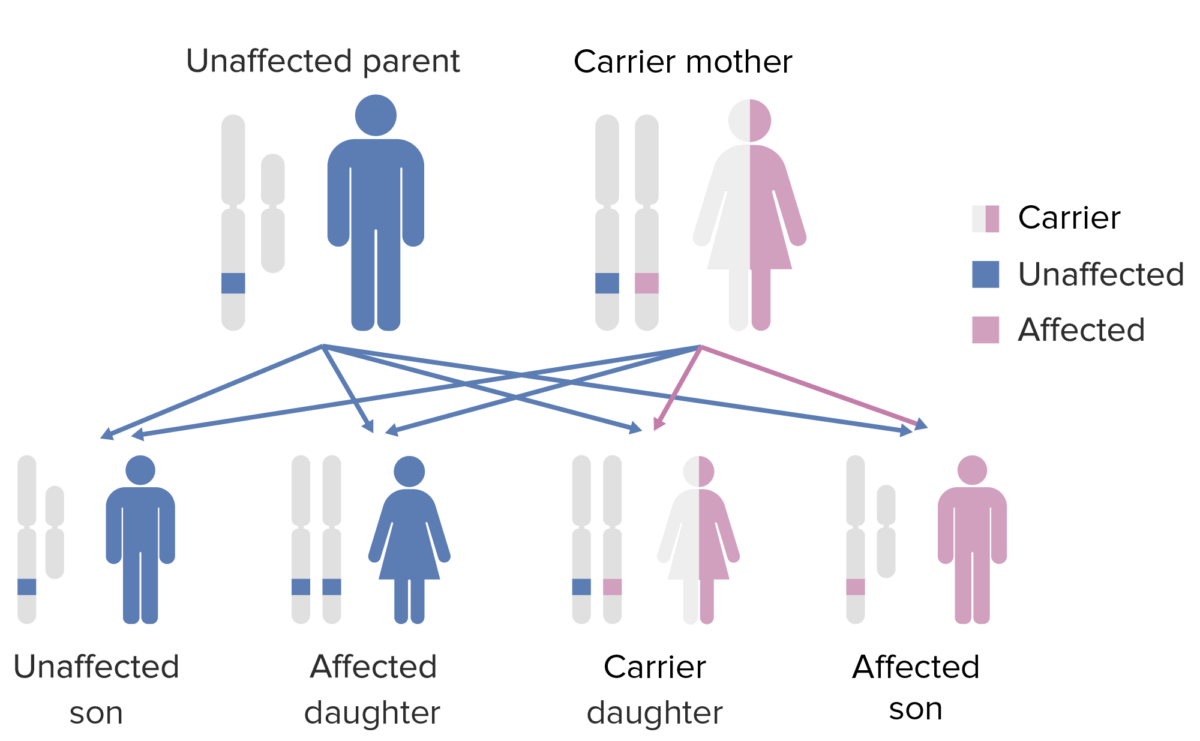
El patrón de herencia de la agammaglobulinemia ligada al cromosoma X:
Tener en cuenta que la madre debe aportar el gen X defectuoso al hijo varón para que éste pueda expresar este fenotipo.
Las siguientes condiciones son diagnósticos diferenciales de la agammaglobulinemia ligada al cromosoma X